Il DMSO possiede numerose qualità che gli consentono di trattare un'ampia varietà di malattie, tra cui:
• Aumenta la circolazione.
• Accelera la guarigione dei tessuti danneggiati (che attualmente ritengo derivi dal miglioramento della circolazione e dalla stabilizzazione dei gel necessari per il processo di guarigione iniziale).
• Risveglia le cellule dormienti intrappolate nella risposta di pericolo cellulare .
• È un potente antiossidante e antinfiammatorio.
• Aumenta il tono parasimpatico (essendo un inibitore dell'acetilcolinesterasi ) e seda i circuiti neurali disfunzionali (consentendo loro di ripristinarsi).
• Riduce efficacemente il dolore (in parte bloccando la trasmissione del dolore e rilassando la muscolatura ).
• Protegge cellule e tessuti da un'ampia varietà di fattori di stress dannosi e letali.
• È un potente sistema di rilascio per altre sostanze terapeutiche che vengono miscelate con esso (in particolare nelle applicazioni topiche).
Tra questi, ritengo che i primi tre (miglioramento della circolazione, rigenerazione dei tessuti e ripristino della risposta di pericolo cellulare, e possibilmente le proprietà antinfiammatorie e antiossidanti del DMSO) siano particolarmente importanti per i disturbi neurologici (per i quali il DMSO è da tempo riconosciuto come efficace nel trattamento) in quanto:
•Il tessuto del sistema nervoso ha il più alto fabbisogno energetico del corpo ed è il più sensibile alla riduzione dell'apporto di sangue (ad esempio, le funzioni del sistema nervoso spesso si "spengono" immediatamente non appena viene interrotto l'apporto di sangue).
•Il tessuto del sistema nervoso è particolarmente vulnerabile alle interruzioni dell'apporto di sangue e, una volta che ciò si verifica, spesso rimane bloccato in uno stato di " penombra " latente, come la risposta di pericolo cellulare (dopo la quale il tessuto alla fine muore). Inoltre, il cervello e il midollo spinale sono tra i tessuti più resistenti alla guarigione e alla rigenerazione in tutto il corpo.
•Dato che gran parte della vita dipende da un sistema nervoso funzionante, perdite parziali di funzionalità dovute a uno dei fattori precedenti creano conseguenze immediatamente evidenti per l'individuo (mentre perdite parziali di funzionalità degli organi interni potrebbero non essere nemmeno rilevate senza esami di laboratorio).
Considerato tutto ciò, ho ipotizzato che il DMSO dovesse migliorare il potenziale zeta, poiché, pur avendo molte proprietà anticoagulanti comprovate (discusse qui ), molti dei cambiamenti che creava erano identici a quelli che si otterrebbero da un miglioramento della microperfusione tramite una maggiore spaziatura dei globuli rossi.
Tuttavia, esaminando la letteratura, ho scoperto che il DMSO (essendo carico in modo neutro) non migliora il potenziale zeta dei globuli rossi e, semmai, lo peggiora leggermente . Allo stesso modo, il DMSO è intrinsecamente viscoso (denso) e aumenta la viscosità dell'acqua strutturandola 1 , 2 , 3 (cosa che si può osservare quando i due si mescolano).
Nota: questa strutturazione esotermica è il motivo per cui il DMSO genera calore quando si mescola con l'acqua.
Tuttavia, le formulazioni DMSO hanno una bassa viscosità, 1 , 2 , 3 , 4 , 5 , 6 , 7 (o diventano caricate negativamente quando preparate in DMSO), il DMSO diminuisce la viscosità degli ioni idrofobici in massa e, soprattutto, riduce l'aggregazione delle cellule del sangue (formazione di fanghi nel sangue) e la viscosità del sangue che credo sia dovuta a:
Si comporta come un agente stabilizzante (promotore) del gel, formando così barriere d'acqua tra le particelle e impedendone l'aggregazione (oltre a far sì che biomolecole come l'urea passino da un comportamento ostile a uno favorevole alla formazione del gel ).
Il DMSO riduce le forze attrattive tra i globuli rossi identificati da Knisely (ad esempio, neutralizzando le proteine aggreganti), consentendo così al potenziale zeta esistente di disperdere le cellule del sangue.
Contrasta inoltre i fattori di agglomerazione che si verificano in condizioni patologiche e che altrimenti causerebbero l'aggregazione delle cellule del sangue. Ad esempio:
• Il DMSO (3%), abbassando la viscosità delle cellule del sangue (e aumentando la mobilità molecolare), ha impedito completamente allo S. aureus di aderire ai globuli rossi (il che, se aderisse, causerebbe l'aggregazione delle cellule del sangue).
• Quando il DMSO è stato miscelato con LPS (per simulare la sepsi), anziché aumentare la viscosità (che è un problema chiave nella sepsi), la viscosità del sangue è diminuita, e si è ulteriormente ridotta una volta aggiunto anche il resveratrolo ⬖ .
• Nel cancro, il DMSO ha impedito la riduzione del potenziale zeta (e della mobilità) che altrimenti si verificherebbe nei macrofagi.
• Ha impedito agli ioni positivi di alterare il potenziale zeta della laponite, che è caricata negativamente.
• Se esposte a radiazioni (raggi gamma), le proteine del cristallino dell'occhio si aggregano e la viscosità aumenta; il DMSO impedisce questo fenomeno.
• Per insediarsi nei polmoni, i batteri che spesso colonizzano i pazienti affetti da fibrosi cistica rilasciano cepacian, un polisaccaride che forma spessi biofilm nel muco polmonare (già denso), rendendo molto più difficile la respirazione per i pazienti con fibrosi cistica. Studi di laboratorio hanno dimostrato che il DMSO è in grado di disgregare gli aggregati di cepacian e dimezzarne la viscosità (il che potrebbe in parte spiegare perché un medico ha riferito che un suo paziente affetto da fibrosi cistica ha avuto miglioramenti radicali dopo il trattamento con DMSO). Inoltre, è stato riscontrato che il DMSO in combinazione con ivacaftor (un farmaco chiave utilizzato per la fibrosi cistica) riduce la viscosità del muco polmonare ispessito dal fumo di sigaretta.
Tutto ciò è stato dimostrato al meglio da un notevole studio del 2009 1 , 2 condotto da un team di ricercatori georgiani che studiavano gli effetti dell'ipertermia (un trattamento antitumorale) sul cervello, poiché, a differenza del resto del corpo, è noto che il cervello e il midollo spinale iniziano a subire danni a temperature più elevate, con disfunzioni neurologiche che iniziano a 40-41 °C e danni termici istologici (ad esempio, necrosi coagulativa) che si verificano nei primati dopo un'ora a 44 °C (motivo per cui 43 °C per 60 minuti è spesso considerato il limite di sicurezza per il trattamento con ipertermia).
Questo studio ha riscaldato direttamente il liquido cerebrospinale dei ratti e ha poi valutato direttamente le conseguenti variazioni del flusso sanguigno nel cervello e le lesioni che ne sono derivate, riscontrando quanto segue:
•L'aumento del calore ha causato un aumento della microcoagulazione (rispecchiando le osservazioni di Knisely e Riddick), con conseguente riduzione del flusso sanguigno e danni al tessuto cerebrale derivanti da tale riduzione.
•Il DMSO ha contrastato tutti questi effetti, preservando il flusso sanguigno e il tessuto cerebrale, mentre, al contrario, il destrano ad alto peso molecolare (una sostanza utilizzata da Knisely per indurre l'agglomerazione del sangue) ha peggiorato l'agglomerazione e il danno cerebrale, dimostrando così perché l'agglomerazione del sangue può causare così tanti disturbi del sistema nervoso e perché il DMSO è in grado di contrastarla.
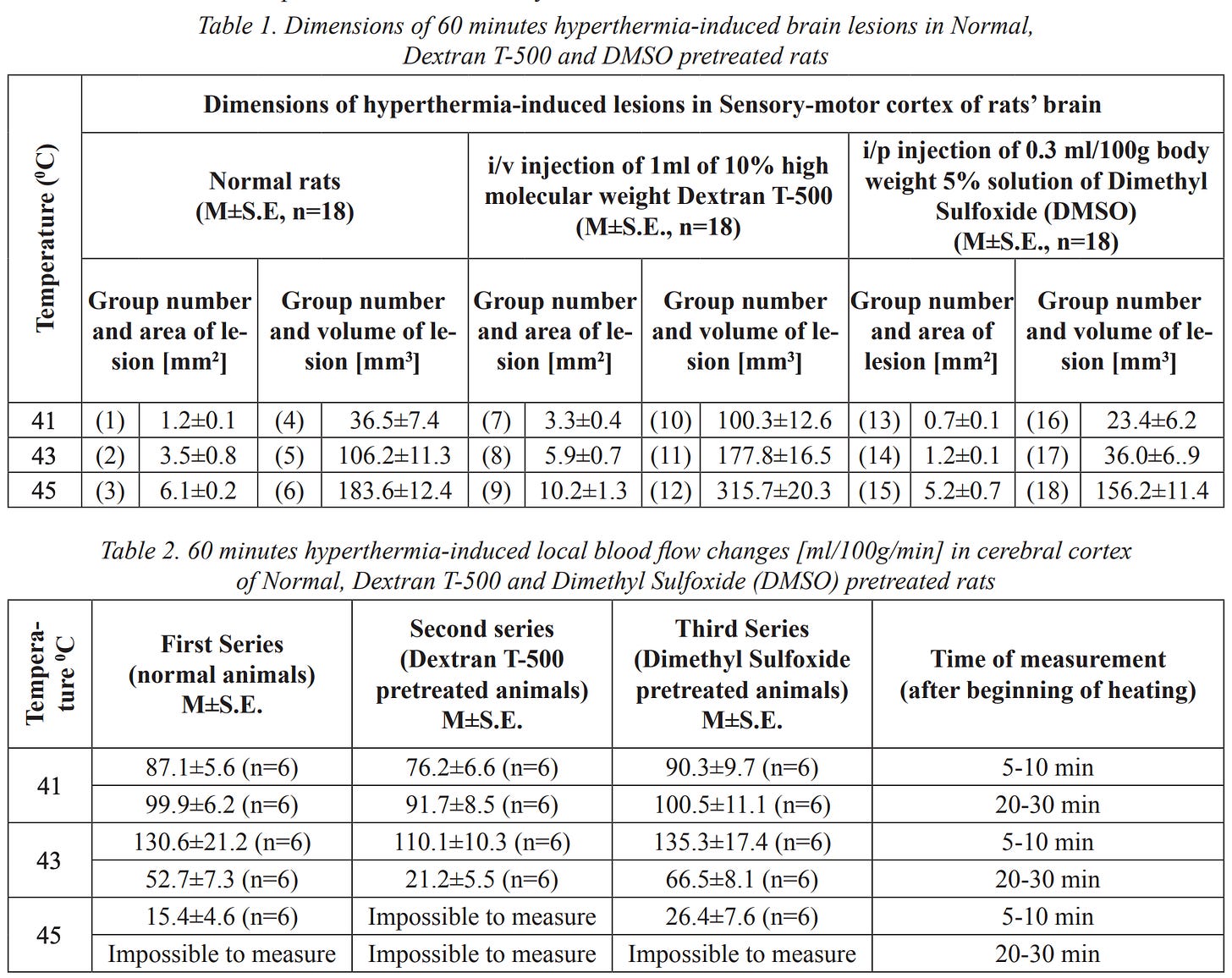 |
| Nota: questi risultati forniscono anche validi argomenti a favore dell'utilizzo del DMSO per mitigare gli effetti negativi del colpo di calore e della febbre alta. |
Inoltre, è stato dimostrato anche che il DMSO:
• Nella microcircolazione intestinale del ratto, per ridurre l'adesione dei leucociti indotta da chemoattrattori (ma non la velocità di rotolamento e il flusso), contrastando così il processo infiammatorio che produce microictus, scoperto da Moulden, in cui i grandi globuli bianchi ostruiscono i vasi sanguigni più piccoli.
• Nei vasi microlinfatici del mesentere intatto del ratto, stimolando costantemente contrazioni fasiche, si è aumentata la percentuale di vasi che presentavano contrazioni fasiche spontanee, passando da un valore basale del 26-42% al 43-59%, raddoppiando approssimativamente la frequenza di contrazione da circa 11 a 25 al minuto. Poiché queste contrazioni stimolano il flusso linfatico, la velocità della linfa è aumentata notevolmente, raddoppiando approssimativamente nel 100% dei vasi (tramite interferometria speckle) e mostrando un aumento del movimento del 40-100% nel 60-64% dei vasi (tramite microscopia diretta), stimolando così la funzione di drenaggio della microcircolazione linfatica. Il DMSO ha inoltre eliminato completamente gli effetti linfocostrittori della tossina stafilococcica batterica (che potrebbero progredire fino all'obliterazione dei microvasi), ha normalizzato il drenaggio linfangionale e ha attenuato l'impatto letale complessivo della tossina. Infine, i ricercatori russi che hanno fatto questa scoperta hanno anche riscontrato che un'esposizione superiore a 15 minuti al DMSO al 30% indurrebbe linfostasi nel 20-40% dei vasi (concentrazioni che non potrebbero mai essere raggiunte in un paziente utilizzando il DMSO). 1 , 2 , 3 , 4
•Per aumentare la circolazione linfatica in numerosi contesti, tra cui la risoluzione della linfostasi nei pazienti con sarcoma di Kaposi e in 115 pazienti con ferite purulente , la facilitazione del drenaggio linfatico ( con stimolazione elettrica e acido ialuronico ), l'aumento della microcircolazione renale e del flusso linfatico , l'aumento del flusso linfatico nell'osteoartrite , l'aumento dose-dipendente del flusso linfatico (come solvente per Daflon endovenoso ), la facilitazione della crescita di nuovi vasi linfatici ( con acido 13-cis retinoico ) e il trattamento del linfedema post-mastectomia (secondo molteplici linee guida, studi e revisioni 1 , 2 , 3 ). Inoltre, un brevetto russo sulla disintossicazione ha inizialmente stimolato il trasporto umorale interstiziale e il drenaggio linfatico applicando DMSO combinato con un enzima proteolitico ai piedi e poi, 30-60 minuti dopo, filtrato il sangue con plasmaferesi.
Nota: il DMSO viene utilizzato anche per somministrare direttamente terapie topiche o iniettabili nel sistema linfatico 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 e per trattare un'ampia gamma di linfadeniti (ad esempio, da vaccino BCG, 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10 tubercolosi, 1 , 2 erisipela emorragica , MIS-C post-COVID , tonsillite e infezioni batteriche che hanno ospedalizzato 61 bambini 1 , 2 ).
Infine, un effetto collaterale comune del DMSO per via endovenosa è l'emolisi osmotica, che colpisce prevalentemente i globuli rossi invecchiati (che la milza eliminerà col tempo). È noto che i globuli rossi invecchiati sono molto più inclini all'agglutinazione e all'aggregazione (in parte perché con l'età perdono la loro carica negativa) e, di conseguenza, la circolazione migliorerà con la loro eliminazione. Questo aiuta a spiegare l'osservazione di Jack De La Torre riguardo ai boli di DMSO per via endovenosa nei pazienti con lesioni cerebrali:
Inoltre, l'ematuria da emolisi osmotica degli eritrociti è stata osservata in tutti i pazienti solo dopo la dose di carico iniziale di DMSO. L'ematuria si è stabilizzata dopo le dosi successive di DMSO. La dose di carico di DMSO non ha altre conseguenze se non quella di ridurre l'ematocrito di circa il 25%, una reazione temporanea che paradossalmente diminuisce la viscosità del sangue e la resistenza vascolare, aumentando al contempo il flusso sanguigno cerebrale .
DMSO e la barriera emato-encefalica
Parallelamente all'aumento della circolazione, il DMSO si diffonde rapidamente nell'organismo e, entro 5 minuti dall'applicazione sulla pelle, può essere rilevato nel sangue, entro 30 minuti in tutti gli organi e entro un'ora nelle ossa; tuttavia, allo stesso tempo, non si accumula nell'organismo dopo un uso prolungato (ad esempio, l'85% viene escreto immodificato nelle urine entro 24 ore ) e praticamente non ne rimane traccia dopo una settimana dalla somministrazione. 1 , 2 , 3
Inoltre, studi su topi e ratti hanno dimostrato che il DMSO a concentrazioni del 10-15% apre reversibilmente la barriera emato-encefalica (BEE), consentendo a proteine come la perossidasi di rafano (HRP), a molti farmaci tra cui pemolina, ketoconazolo (con concentrazioni cerebrali che aumentano di 9 volte) o il farmaco per il Parkinson L-dopa (che aumenta i livelli di dopamina nelle aree tubero-infundibolari e neostriatali e ulteriormente potenziato se combinato con carbidopa), ai lisosomi che trasportano farmaci e agli amminoacidi come la tirosina di raggiungere il tessuto cerebrale in quantità maggiori rispetto a quanto avverrebbe senza DMSO. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 , 9 , 10 , 11 , 12 , 13 , 14 , 15 , 16 , 17 , 18 , 19 , 20
Il DMSO ha anche aumentato il trasferimento di aminoacidi attraverso lo spazio subaracnoideo nel tessuto corticale sottostante di circa il 57% , e nei pulcini neonati, il DMSO per via endovenosa ha aumentato le concentrazioni cerebrali di adrenalina e noradrenalina di circa il 35-39% e ne ha intensificato gli effetti centrali. 1 , 2 Allo stesso modo, nei cani, il DMSO per via endovenosa a velocità di infusione crescenti ha raggiunto una concentrazione nel liquido cerebrospinale circa la metà della corrispondente concentrazione plasmatica , confermando una penetrazione (più lenta) attraverso la barriera emato-encefalica nel sistema nervoso centrale. Questa capacità di facilitare la somministrazione di farmaci al cervello è alla base del potenziale terapeutico del DMSO per i disturbi neurologici (ad esempio, il morbo di Parkinson) e ha portato ad essere raggruppato con il mannitolo come agente clinico per migliorare la somministrazione di farmaci al cervello . Allo stesso modo, il DMSO è stato incorporato in formulazioni di nanoparticelle mirate al cervello, come le micelle di poloxamero mediate dal glucosio, che hanno mostrato un trasporto significativamente maggiore attraverso un modello di barriera emato-encefalica rispetto alle micelle ordinarie. 1 , 2
Nota: ci sono risultati contrastanti sull'apertura temporanea della BBB da parte del DMSO (ad esempio, questi otto studi hanno scoperto che non lo faceva, 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8 questo ha scoperto che l'apertura della BBB richiedeva l'1% o più di DMSO, un altro ha scoperto che aveva un effetto minimo sul trasporto della dopamina) questi hanno scoperto che l'apertura era anche problematica, 1 , 2 mentre nei ratti e nei conigli le infusioni di DMSO nelle carotidi non hanno danneggiato la BBB, le arterie o il cervello 1 , 2 e una revisione veterinaria del 1985 ha ugualmente notato che il DMSO consente ad alcune sostanze ma non ad altre di attraversare la BBB.
Negli studi di risonanza magnetica sui topi, il DMSO si è accumulato a concentrazioni 1,5 volte superiori nei glioblastomi rispetto al tessuto cerebrale normale con un washout 2,2 volte più lungo, creando chiari "punti caldi" del tumore. A differenza del gadolinio, un mezzo di contrasto tossico, il DMSO attraversa liberamente la barriera emato-encefalica intatta, consentendo la visualizzazione di tumori di basso grado invisibili alla risonanza magnetica convenzionale; inoltre, durante la chemioterapia, le riduzioni della ritenzione di DMSO segnalano la risposta al trattamento prima delle variazioni volumetriche rilevate con la risonanza magnetica. 1 , 2 , 3 , 4 , 5 , 6 È stato anche dimostrato che il DMSO migliora la penetrazione della luce nel tessuto cerebrale, ottimizzando le tecniche diagnostiche ottiche rilevanti per alcune patologie neurologiche. 1 , 2
DMSO e disturbi psichiatrici
Due delle critiche più comuni rivolte alla psichiatria riguardano il fatto che i suoi farmaci (altamente tossici) non curano la malattia di base, rendendo necessaria una gestione sintomatica a vita, e che reali problemi biologici (ad esempio, i danni causati dal vaccino anti-COVID) vengono regolarmente diagnosticati erroneamente come disturbi psichiatrici primari. Entrambi i problemi derivano dall'erronea convinzione che la maggior parte delle patologie psichiatriche abbia origine esclusivamente nella mente, quando in realtà molte hanno una chiara base biologica (neurologica).
La mia prospettiva deriva dall'aver osservato ripetutamente la comparsa di sintomi psichiatrici in seguito a lesioni cerebrali e dall'aver constatato che le terapie mediche che ripristinano la salute cerebrale migliorano anche i problemi psichiatrici. Ad esempio, una delle mie terapie preferite, l'irradiazione del sangue con raggi ultravioletti , agisce migliorando la circolazione, riducendo l'infiammazione e riattivando le cellule dormienti, effetti che si verificano anche con il DMSO . Poiché questi processi sono alla base di numerose patologie, così come un'ampia letteratura scientifica supporta l'efficacia dell'irradiazione del sangue con raggi ultravioletti in una vasta gamma di condizioni, comprese quelle psichiatriche, lo stesso vale anche per il DMSO (come dimostrerò nel corso di questo articolo).
Nel processo di scavo di ogni articolo esistente sul DMSO, ho scoperto un team russo (presso l' Istituto di Attività Nervosa Superiore e Neurofisiologia dell'Accademia Russa delle Scienze ) che ha prodotto alcune delle migliori prove che io abbia mai trovato a sostegno di questa teoria. 1 , 2 , 3 , 4 , 5 , 6 , 7 , 8
In breve, nel tentativo di individuare una causa biologica dei disturbi psichiatrici (che presentano una vasta gamma di cause apparentemente non correlate), hanno scoperto che lo stress cronico, responsabile dei disturbi psichiatrici, è accompagnato da un'alterazione della circolazione sanguigna cerebrale, che innesca una serie di processi degenerativi, soprattutto quando la capacità dell'individuo di compensare lo stress acuto a breve termine viene sopraffatta dallo stress cronico e prolungato.
Per studiare questo fenomeno, hanno indotto ripetutamente la nevrosi negli animali utilizzando fattori di stress prolungati (rumore bianco, lampi di luce e scosse elettriche per oltre 3 settimane), quindi, utilizzando la biomicroscopia (finestra cranica) e la clearance dell'idrogeno, hanno misurato direttamente il flusso sanguigno nel territorio dell'arteria cerebrale media e, infine, hanno esaminato direttamente i cervelli.
Nota: nevrosi (невроз) è un termine psichiatrico obsoleto. In questo contesto di epoca sovietica, descrive un'alterazione dell'attività nervosa superiore causata da stress cronico che sopraffà la capacità di adattamento della persona. Gli equivalenti moderni includono il disturbo d'ansia generalizzato, il disturbo misto depressivo e ansioso (ICD-11), la nevrastenia e il disturbo dell'adattamento con umore ansioso o depresso.
Da ciò hanno ricavato:
•Il cervello riceve normalmente un flusso sanguigno per grammo di tessuto 5-7 volte superiore rispetto alla maggior parte degli altri organi, a causa del suo eccezionale fabbisogno energetico. Lo stress acuto in genere causa un aumento a breve termine del flusso sanguigno cerebrale, ma lo stress cronico prolungato (che porta alla nevrosi) produce una diminuzione sostenuta che persiste per 4-6 settimane dopo la fine dello stressor. Questa riduzione causa ipossia circolatoria, aumento del lattato cerebrale, diminuzione dell'attività della caspasi-3 e della Na,K-ATPasi, alterazione della respirazione mitocondriale (inclusa la riduzione dell'attività della succinato deidrogenasi e della NADH deidrogenasi) e aumento della produzione di specie reattive dell'ossigeno (ROS) (e negli animali incapaci di adattarsi passando dall'ossidazione dell'acido succinico all'ossidazione del NADH, la resistenza allo stress è notevolmente ridotta). L'ipossia risultante aumenta anche l'attività della citocromo ossidasi (del 35-40%) e innesca la biogenesi mitocondriale, seguita dalla perossidazione lipidica (LPO) innescata dalle ROS. 1 , 2 , 3 , 4 Nota: il cervello è particolarmente vulnerabile a questa cascata a causa del suo metabolismo e della sua richiesta di ossigeno eccezionalmente elevati, nonché dell'alto contenuto di acidi grassi polinsaturi (ossidabili) nelle membrane cellulari.
•Nelle fasi iniziali della nevrosi, lo stress acuto, una risposta protettiva aspecifica, inibisce la perossidazione lipidica (LPO), accumula fosfolipidi facilmente ossidabili, diminuisce il contenuto di colesterolo e aumenta l'attività di eliminazione dei radicali superossido (in parte dovuta agli ormoni dello stress che agiscono come spazzini di radicali). Con il protrarsi dello stress cronico, questa fase protettiva viene sopraffatta, portando all'attivazione dell'ossidazione lipidica da radicali liberi, alla progressiva deplezione dei fosfolipidi, all'accumulo di colesterolo e a un aumento delle proteine ossidate . Questi cambiamenti bifasici della membrana inizialmente aumentano la resistenza a un'ulteriore perossidazione, ma alla fine rendono le membrane più vulnerabili con il proseguire dello stress. 1 , 2 , 3 , 4 Nota: questo andamento bifasico è stato osservato anche nelle donne con dismenorrea (dopo 12 ore di dolore, i livelli plasmatici delle basi di Schiff erano ridotti di quasi due terzi, mentre dopo 12-24 ore erano quasi il doppio rispetto ai valori di controllo).
• Gli adattamenti successivi allo stress cronico sono più specifici e le modifiche delle membrane e dei radicali liberi mostrano spesso un'asimmetria interemisferica che varia a seconda del tipo di comportamento. Ad esempio, nello stress acuto, gli animali con elevata reattività emotiva e risonanza emotiva tendono a una LPO bilanciata o a predominanza destra (come i ratti sensibili allo stress che eccellono nei labirinti), mentre gli animali con bassa reattività presentano una maggiore LPO a sinistra (come i ratti resistenti allo stress che non sono bravi nei labirinti).
•Questi cambiamenti molecolari sono accompagnati da evidenti disturbi fisiologici: pressione sanguigna sistolica elevata e fluttuante, interruzione e riduzione del flusso sanguigno cerebrale locale, perdita di specificità funzionale ( equalizzazione del flusso sanguigno tra le strutture cerebrali ) e un cambiamento comportamentale verso un comportamento passivo-difensivo. Poiché lo stress e l'iperattività simpatica possono causare questi disturbi autonomici, i ricercatori hanno concluso che la conseguente restrizione del flusso sanguigno cerebrale contribuisce a molti dei sintomi osservati nella nevrosi.
Nota: una delle mie modalità preferite ( la terapia neurale ) agisce neutralizzando i disturbi autonomici e spesso produce risposte rapide e significative nelle malattie complesse, il che, a mio avviso, è correlato al processo patologico descritto dai ricercatori russi.
• Hanno anche scoperto che il rilascio locale di noradrenalina nell'ipotalamo laterale funziona come parte di un sistema depressore che aiuta a normalizzare la pressione sanguigna elevata. Durante lo stress acuto, la velocità di ritorno alla pressione sanguigna basale dipendeva dall'intensità di questa risposta noradrenergica locale nell'ipotalamo laterale. Pertanto, quando questo meccanismo è compromesso, lo stress ripetuto può portare a un'instabilità emodinamica prolungata che, nel tempo, può contribuire alla disregolazione dell'autoregolazione cerebrale e a riduzioni sostenute del flusso sanguigno cerebrale (che a sua volta danneggia l'ipotalamo, creando una spirale discendente verso la malattia cronica).
Nota: la maggior parte dei casi di pressione sanguigna cronicamente elevata non ha una causa nota. Questo quadro potrebbe spiegare una causa chiave non riconosciuta (insieme a un altro motivo per cui il ripristino del potenziale zeta migliorerà la pressione sanguigna , in quanto ciò ripristinerà il flusso sanguigno all'ipotalamo). Inoltre, dovrei notare che alcuni guaritori olistici hanno riportato un successo significativo nel trattamento dell'eccessiva attività simpatica intervenendo sulla funzione ipotalamica.
•Il normale flusso sanguigno cerebrale è di circa 50 ml/100 g/min; nella nevrosi cronica scende al di sotto dei 30 ml /100 g/min . Anche i vasi cerebrali perdono la capacità di autoregolazione: dopo l'occlusione carotidea bilaterale, gli animali normali mostrano una dilatazione arteriosa generalizzata, mentre gli animali con nevrosi presentano risposte arteriose e venose miste (ad esempio, nelle arteriole il 54% si dilata, il 21% si restringe, il 25% non subisce variazioni) con frequenti contrazioni spastiche, deformazioni a bottiglia, flusso interrotto e reazioni vascolari piali alterate, con conseguente equalizzazione relativa della velocità del flusso sanguigno in tutte le strutture studiate (indicando una perdita di specificità funzionale, che ritengo abbia un'enorme rilevanza clinica poiché alcune tradizioni mediche associano questo cambiamento circolatorio all'avvicinarsi della morte). Nota: in molti casi , l'emodinamica cerebrale non si ripristina mai completamente dopo il periodo di stress cronico.
•Questi cambiamenti emodinamici sono paralleli all'omogeneizzazione dell'attività EEG osservata nella nevrosi. La biomicroscopia ha confermato alterazioni microstrutturali compatibili con l'ipossia, tra cui edema perivascolare e pericellulare, vasi tortuosi, neuroni scuri, cellule acidofile, proliferazione microgliale e danno ippocampale (in particolare soma rimpicciolito, nuclei alterati e dendriti a cavatappi in CA3; perdita cellulare del 2,7-7,1% in CA1, che si avvicina alla soglia per il deterioramento cognitivo e la demenza).
•Il processo danneggia selettivamente i recettori β-adrenergici del cervello (che per circa una settimana hanno mostrato una ridotta affinità recettoriale, compensata da un aumento del numero di recettori, con la densità recettoriale elevata che persisteva anche dopo tre settimane), la corteccia sensomotoria (strato V) e l'ippocampo (nello strato piramidale, in particolare nel campo CA3 ).
•Nel modello di stress cronico emotivo-doloroso sono state identificate tre fasi della sindrome generale di adattamento: (1) ricerca iniziale di un funzionamento ottimale con difetti viscerali residui, comportamento dominato dalla paura e pressione sanguigna labile, della durata di una settimana; (2) stabilizzazione autonomica parziale ma continua deplezione dei fosfolipidi ("usura locale"); (3) esaurimento con rottura della regolazione autonomica, attivazione della LPO e profonda rottura delle membrane a livello di neuroni, glia e sinapsi, che contribuisce al crollo dell'attività nervosa superiore, che è stata descritta come "adattamento patologico con un alto costo strutturale".
Essi quindi:
•Ha sottolineato che la reazione interna di un individuo agli stressor, piuttosto che lo stressor stesso, è fondamentale (“... non importa quali fatti ci vengano riportati, ciò che conta è come reagiamo ad essi; questa è la questione principale ”) e l'ha collegata all'osservazione che molte malattie derivanti da stress psicoemotivo cronico sono caratterizzate da disturbi autonomici (vascolari), stati ipossici e gravi alterazioni dei processi metabolici, che spesso si manifestano come disregolazione autonomica/vascolare, ipossia e disturbi metabolici.
Nota: il non anglofono che ha coniato il concetto medico di stress ha successivamente affermato di aver usato la parola sbagliata e di aver inteso usare il termine strain (come un sistema si deforma in risposta allo stress).
•Si è osservato che, sebbene molti individui raggiungano la nevrosi conclamata, molti di più si trovano in una fase pre-nevrotica di notevole stress senza scompenso completo e trarrebbero grande beneficio da interventi terapeutici precoci nel corso della malattia.
•Hanno evidenziato che gli effetti dello stress cronico da loro osservati erano simili a quelli riscontrati dopo ictus , infarti o lesioni cerebrali traumatiche e, in molti casi, hanno utilizzato con successo le stesse terapie per entrambi (ad esempio, pantenolo ⬖ ).
Per affrontare la nevrosi:
•I ricercatori hanno utilizzato per primi agenti con proprietà antiipossiche e antiossidanti (ad esempio, carnosina , sostanza P , fenosano K o antiossidanti fenolici sintetici 1 , 2 ) e hanno scoperto che questi interventi prevenivano e trattavano efficacemente la nevrosi sperimentale negli animali (mentre gli animali non trattati sviluppavano costantemente nevrosi e mostravano una scarsa ripresa).Nota: altri agenti come il pantenolo ⬖ hanno fornito solo miglioramenti temporanei. Inoltre, hanno avuto un successo significativo anche con l'alcol (uno scavenger di radicali idrossilici), fornendo una nuova spiegazione del perché l'alcol offra un certo sollievo dalla depressione cronica. In particolare, lo stress cronico ha ridotto l'attività della Na,K-ATPasi cerebrale (come dettagliato sopra), e uno studio separato sulla Na,K-ATPasi cerebrale ha scoperto che mentre sia il DMSO che l'etanolo scaveranno i radicali idrossilici, l'etanolo destabilizzerà ulteriormente l'enzima mentre il DMSO lo stabilizzerà, il che potrebbe spiegare perché il DMSO fornisce un beneficio duraturo laddove l'alcol allevia solo temporaneamente i sintomi (mentre parallelamente, Riddick ha scoperto che l'alcol aumentava la formazione di sedimenti nel sangue).
Dopo aver testato diversi agenti, i ricercatori hanno ottenuto un grande successo con la terapia a ioni negativi (che ha un pronunciato effetto antiipossico). Quando presenti durante uno stress acuto (ad esempio, immobilizzazione), gli ioni negativi hanno completamente impedito le alterazioni patologiche cerebrali in tutti gli animali, indipendentemente dal tipo comportamentale, compresa la preservazione dell'attività degli enzimi ossidativi nella corteccia sensomotoria e la normalizzazione dei parametri comportamentali e autonomici (frequenza cardiaca, pressione sanguigna e respirazione). Effetti protettivi simili sono stati osservati con l'acido succinico ⬖ (30 mg/kg per via orale al giorno per 8 giorni), che ha anche preservato il comportamento di orientamento dopo un attacco cardiaco. In particolare, i ratti con un tipo comportamentale attivo hanno mostrato una maggiore resistenza naturale all'ipossia cerebrale, esibendo aumenti più rapidi del flusso sanguigno cerebrale locale e della tensione di ossigeno cerebrale durante lo stress.
Nota: gli ioni positivi nell'aria sono stati ampiamente collegati a condizioni psichiatriche . Credo che ciò sia dovuto al fatto che gli ioni positivi compromettono il potenziale zeta e quindi riducono la microcircolazione cerebrale (mentre gli ioni negativi la ripristinano).
Alla fine, ottennero il massimo successo combinando il DMSO orale (un potente antiossidante) con la vitamina E ( alfa-tocoferolo ) , scoprendo che l'efficacia di questa combinazione superava quella delle due sostanze somministrate separatamente (ad esempio, per problemi autonomici o comportamentali ). Attribuirono questo risultato al fatto che il DMSO potenziava la capacità antiossidante della vitamina E, poiché poteva trasportarla rapidamente alle membrane cellulari prima che perdesse la sua capacità antiossidante reagendo con altre sostanze nell'organismo ( supportato dalla riduzione dei prodotti di ossidazione dei radicali liberi, dall'aumento dell'attività di neutralizzazione del superossido nel cervello e nel siero sanguigno, dall'aumento del contenuto di fosfolipidi cerebrali e dalla normalizzazione del contenuto di colesterolo cerebrale). Infine, nel 1999, comunicarono che questi risultati avevano iniziato a essere replicati in studi clinici approvati dal governo presso l'Accademia Medica di Mosca.
Sebbene si potrebbe dire molto sulla loro ricerca, una delle lezioni fondamentali che ho appreso è stata una delle spiegazioni meccanicistiche più chiare che abbia mai incontrato su cosa facciano effettivamente gli adattogeni (un termine applicato a molti prodotti naturali), dato che gli agenti che hanno contrastato efficacemente l'intero processo di stress sono stati esplicitamente caratterizzati dai ricercatori come "adattogeni".
Nota: per compilare il riassunto di cui sopra e rappresentare accuratamente i risultati, ho letto oltre 50 articoli (molti dei quali omettevano dettagli chiave) e ho fatto del mio meglio per integrare le loro scoperte con le attuali conoscenze scientifiche in fisiologia.
Con questa premessa (e un'ulteriore analisi dell'importanza del drenaggio circolatorio, che verrà discussa nella sezione dedicata alla sclerosi multipla), esaminiamo ora come queste proprietà permettano al DMSO di influenzare un'ampia gamma di disturbi neurologici e psichiatrici.
malattia di Parkinson
Il morbo di Parkinson è causato dalla progressiva perdita dei neuroni che producono dopamina nella substantia nigra. La ricerca in questo campo è stata rivoluzionata all'inizio degli anni '80, quando i consumatori di droghe ricreative che si iniettavano eroina sintetica di scarsa qualità svilupparono rapidamente gravi sintomi simili al Parkinson a causa della contaminazione con MPTP, una sostanza il cui metabolita attivo (MPP+) colpiva specificamente quei neuroni, rendendo possibile riprodurre in modo affidabile il Parkinson negli animali da laboratorio. A ciò seguì la scoperta che un erbicida (paraquat) era molto simile all'MPP+, che un altro pesticida (rotenone) causava danni simili ai neuroni, che diversi pesticidi erano collegati a un rischio maggiore di Parkinson (come gli organofosfati) e che anche la 6-OHDA era in grado di indurre il Parkinson in modo affidabile.
Nota: una delle principali problematiche relative al glifosato (Roundup) è che, pur essendo tossico, gli erbicidi che ha in gran parte sostituito, come il paraquat, sono più tossici.
Numerosi studi hanno dimostrato che il DMSO contrasta direttamente la neurotossicità di questi agenti che causano il Parkinson (ad esempio, negli studi sugli organofosfati menzionati in precedenza, il DMSO ha ripetutamente ridotto la mortalità, accelerato la detossificazione degli organofosfati e protetto la funzione neuromuscolare). In particolare, uno studio caso-controllo sul morbo di Parkinson a esordio precoce (63 casi, 68 controlli) ha rilevato che gli individui affetti da Parkinson avevano una probabilità dieci volte inferiore di essere stati esposti al DMSO rispetto ai soggetti di controllo sani, suggerendo che l'esposizione al DMSO è associata a una riduzione di circa 10 volte del rischio di malattia (e quindi potrebbe avere un effetto protettivo). Al contrario, lo stesso studio ha rilevato che l'esposizione agli insetticidi aumentava il rischio di quasi 6 volte, l'esposizione a fumigazioni in abitazioni di oltre 5 volte e l'esposizione agli erbicidi di oltre 3 volte: risultati coerenti con l'ampia letteratura epidemiologica che collega l'esposizione ai pesticidi al morbo di Parkinson.
Nota: questo studio ha anche rilevato che il fumo era associato a un ridotto rischio di malattia di Parkinson, un risultato che si allinea con decenni di evidenze epidemiologiche che collegano l'esposizione alla nicotina a una minore incidenza della malattia di Parkinson, conferendo credibilità alla metodologia dello studio.
Il DMSO ha dimostrato direttamente effetti neuroprotettivi in diversi modelli di Parkinson. Negli animali, il DMSO ha soppresso il danno nigrostriatale indotto dai radicali idrossilici da MPTP, 1 , 2 , 3 , 4 e nei ratti con Parkinson indotto da rotenone, il DMSO ha migliorato la morfologia dei neuroni CA1 e CA3 dell'ippocampo , ripristinando le cellule piramidali e i corpi di Nissl danneggiati dal rotenone e normalizzando la loro attività elettrica. Il DMSO ha anche protetto gli astrociti dalla tossicità indotta da MPP+ riducendo la perossidazione lipidica e il danno metabolico, ha protetto la glutammina sintetasi gliale dal danno da radicali idrossilici indotto da MPP+, ha protetto le cellule di neuroblastoma umano SH-SY5Y dalla citotossicità indotta da 6-OHDA e ha ridotto sia la perossidazione lipidica che la formazione di carbonili proteici negli omogenati cerebrali di ratto da cloruro ferroso o perossido di idrogeno e ha ridotto separatamente la produzione di radicali idrossilici durante l'autoossidazione di 6-OHDA e la formazione di prodotti dopaminergici idrossilati. 1 , 2
Nota: in uno studio sui topi , il DMSO intraperitoneale non ha protetto dalla deplezione di dopamina indotta da MPTP, indicando che i suoi effetti neuroprotettivi possono dipendere dalla via, dalla tempistica o dalla dose di somministrazione.
È interessante notare che il DMS (metabolita del DMSO presente in natura e responsabile dell'odore) a concentrazioni quasi fisiologiche ha protetto i neuroni dall'apoptosi indotta sia da 6-OHDA che da MPP+, con un effetto dipendente da MsrA (l'enzima che converte il DMS in DMSO), suggerendo che il ciclo endogeno DMS-DMSO funzioni come parte della difesa antiossidante naturale dell'organismo contro la neurodegenerazione dopaminergica. 1 , 2 Questo, a sua volta, solleva un interessante dilemma, poiché ho ricevuto alcune segnalazioni di pazienti affetti da Parkinson che hanno avuto risposte significative al DMSO, ma che poi hanno interrotto il trattamento a causa dell'odore che impediva i rapporti sessuali con il coniuge. Il mio primo pensiero è stato quello di raccomandare una formulazione di DMSO a basso odore (discusso qui ), ma se il DMS svolge un ruolo terapeutico chiave nella malattia di Parkinson, questo approccio potrebbe non essere praticabile.
Nota: quello studio ha anche rilevato che il DMS proteggeva dalla perossidazione lipidica indotta da H₂O₂ e dalla produzione di superossido generata dall'antimicina A.
Inoltre, il DMSO ha annullato il blocco completo dell'assemblaggio dei microtubuli dalla tubulina purificata in vitro causato dal rotenone , un risultato di diretta rilevanza per il morbo di Parkinson, poiché la disorganizzazione dei microtubuli compromette il trasporto assonale e contribuisce alla morte dei neuroni dopaminergici. Analogamente, una monografia russa di fisioterapia raccomandava impacchi topici di novocaina con DMSO per patologie neurologiche, tra cui il morbo di Parkinson, e un brevetto proponeva il DMSO come potenziatore transdermico per un cerotto a base di tossina botulinica per il trattamento della spasticità associata a morbo di Parkinson, paralisi cerebrale, distonia e sclerosi multipla.
Nota: un gran numero di studi (che saranno discussi più avanti in questa serie) dimostrano che il DMSO stabilizza i microtubuli e probabilmente è responsabile di alcune delle sue qualità neuroprotettive.
Un vasto numero di agenti in combinazione con il DMSO ha inoltre mostrato benefici terapeutici in modelli di morbo di Parkinson.
La curcumina ⬖ ha protetto i neuroni dopaminergici della substantia nigra, ridotto l'attivazione di iNOS e delle cellule gliali e potenziato le vie neuroprotettive (IGF-1/Akt/FoxO3a). 1 , 2
La peoniflorina ⬖ ha ripetutamente ridotto l'espressione dell'α-sinucleina, diminuito la formazione di corpi di Lewy e protetto i neuroni dopaminergici in numerosi studi. 1 , 2 Ha inoltre inibito l'iperattivazione microgliale, aumentato la secrezione di BDNF e GDNF e promosso la differenziazione delle cellule staminali neurali in neuroni dopaminergici. 1
L'icariside II ⬖ ha indotto le cellule staminali mesenchimali amniotiche umane a differenziarsi in cellule simili a neuroni dopaminergici (ottimale a 3–10 μmol/L tramite la via di segnalazione PI3K). In un altro protocollo, il DMSO ha contribuito a differenziare le iPSC in progenitori dopaminergici per la terapia con cellule staminali del morbo di Parkinson.
I ginsenosidi Rg1 ⬖ e Rg3 ⬖ hanno entrambi attenuato significativamente la perdita di neuroni dopaminergici, la neuroinfiammazione e l'accumulo di α-sinucleina. 1 , 2 , 3 , 4
Il geniposide ⬖ ha ridotto i livelli di α-sinucleina e ha prevenuto la perdita di neuroni dopaminergici modulando l'asse miR-21/LAMP2A, mentre il ginkgolide B ⬖ ha ridotto in modo simile l'espressione di α-sinucleina attraverso la via correlata miR-207/LAMP2A. 1 , 2 L'ambroxolo ha aumentato l'attività della β-glucocerebrosidasi e ridotto i livelli di oligomeri di α-sinucleina, ripristinando la vitalità cellulare e la funzione mitocondriale nei neuroni dopaminergici. I polifenoli ⬖ hanno ridotto l'aggregazione di α-sinucleina indotta tramite risposte antiossidanti mediate da NRF2. L'acido carnosico ⬖ ha attenuato la neurotossicità del 6-OHDA mediante la sovraregolazione della parkina e il ripristino della clearance proteasomica delle proteine ubiquitinate in modelli cellulari e animali di PD.
L-sulforafano ⬖ disciolto in DMSO ha attivato la via NRF2 nelle cellule derivate da pazienti affetti da malattia di Parkinson, ripristinando i loro livelli carenti di glutatione: uno dei pochi studi che utilizza cellule di pazienti reali.
In modo del tutto singolare , NAMI-A, un complesso di rutenio-DMSO a bassa tossicità, ha inibito l'aggregazione dell'α-sinucleina e le interazioni con la membrana con affinità submicromolare, ha disassemblato le fibrille preformate, ha abolito la citotossicità dell'α-sinucleina verso le cellule neuronali e ha attenuato la neurodegenerazione e i deficit motori in un modello di Parkinson nel ratto, fornendo una nuova base per la progettazione di complessi di rutenio-DMSO che agiscono sulla patologia indotta dall'α-sinucleina attraverso un meccanismo distinto da quello degli agenti organici.
Nei modelli MPTP, il tanshinone IIA ⬖ ha preservato circa il 75% dei neuroni dopaminergici riducendo al contempo l'attivazione microgliale; la tetrametilpirazina ⬖ ha prevenuto i deficit motori e la perdita di neuroni tramite la via Nrf2; il 6-idrossi-1H-indazolo ha protetto il 90-93% dei neuroni dopaminergici dalla morte; la baicaleina ⬖ ha ridotto in modo dose-dipendente il comportamento rotatorio (un indicatore chiave di compromissione motoria), la neuroinfiammazione e l'apoptosi dei neuroni dopaminergici tramite Wnt/β-catenina; la neferina ⬖ ha migliorato i disturbi motori nei topi e ridotto la neuroinfiammazione e l'α-sinucleina nella substantia nigra; SB239063 (un inibitore della p38 MAPK) ha protetto i neuroni TH-positivi; NESS 0327 (un antagonista del recettore CB1) ha migliorato i deficit motori; I nuovi inibitori della chinasi c-Abl hanno superato il nilotinib nel bloccare l'apoptosi indotta da MPP+; GW5074 ha impedito la perdita di neuroni TH-positivi in topi geneticamente modificati per avere il Parkinson. Nei topi con lesione della via nigrostriatale, sia l'inibizione di ERK ( U0126 ) che l'inibizione di PDGFRα ( AG1296 ) hanno ridotto l'attivazione gliale e la cicatrizzazione, con U0126 che ha anche migliorato gli esiti neurocomportamentali a lungo termine.
Nei topi con malattia di Parkinson indotta da LPS , il pazopanib ha protetto i neuroni dopaminergici sopprimendo TNF-α, PGE2 e IL-6 tramite la via di segnalazione MEK4-JNK-AP-1, mentre la rapamicina ha ridotto la neuroinfiammazione potenziando il metabolismo lipidico microgliale.
NBP (un farmaco cinese per l'ictus) ha salvato i neuroni dopaminergici del 30% e le terminazioni dopaminergiche striatali del 49%. Il carvacrolo ⬖ (presente negli oli di origano e timo) ha avuto un effetto neuroprotettivo tramite l'inibizione di TRPC1 nei neuroni dopaminergici e l'attivazione di TRPA1 negli astrociti. Dasatinib e resveratrolo ⬖ in combinazione hanno migliorato l'apprendimento, la memoria, la coordinazione motoria e ridotto l'ansia. MOTS-c ⬖ ha migliorato la funzione motoria , invertito la perdita di neuroni TH-positivi e attivato la via antiossidante Nrf2/Keap1 nei ratti con malattia di Parkinson trattati con rotenone. Puerarina ⬖ ha attenuato il comportamento rotatorio e aumentato l'espressione di DAT, VMAT2 e TH nei ratti con malattia di Parkinson trattati con rotenone. Un inibitore della caspasi ha ridotto la perdita di neuroni e migliorato il comportamento rotatorio nei ratti trattati con 6-OHDA, sebbene il blocco dell'apoptosi abbia innescato una necroptosi gliale compensatoria.
Shuimuheningfang ⬖ ha migliorato i sintomi motori e non motori in 80 pazienti affetti da malattia di Parkinson e ha ridotto l'α-sinucleina nei topi modello, 1 , 2 mentre i granuli composti di Dihuang ⬖ (con un inibitore di JNK) hanno ridotto il comportamento rotatorio e protetto i neuroni dopaminergici nei ratti trattati con 6-OHDA.
Nei modelli di malattia di Parkinson in C. elegans , l'estratto di foglie d'olivo ⬖ ha protetto fortemente i neuroni dopaminergici dalla tossicità del 6-OHDA (fino al ~56% in meno di degenerazione), mentre l'oleuropeina, ⬖ l'acido oleanolico, ⬖ il tirosolo, ⬖ il 3-idrossitirosolo, ⬖ lo zafferano, ⬖ il Polygonum multiflorum, ⬖ e lo Ziziphus jujuba ⬖ hanno fornito ciascuno una protezione significativa.
Altri agenti che mostrano effetti neuroprotettivi nei modelli di PD includono guaranà ⬖ (contro il rotenone nelle cellule SH-SY5Y), olio di krill antartico ⬖ (migliora l'attività locomotoria e i neuroni dopaminergici nel pesce zebra), luteina ⬖ (migliora i risultati cognitivi e motori nei ratti in modo dose-dipendente), composti di citocalasina da funghi endofitici (contro MPP+), estratto di Erythrina velutina , ⬖ acido rizonico ⬖ e derivati di xilochetale ⬖ (contro il danno mediato da 6-OHDA o ROS), butirrato di sodio ⬖ ( un inibitore di HDAC che ripristina epigeneticamente il trasportatore della dopamina e l'espressione di VMAT2 contro il rotenone e MPP+), allopregnanolone (promuove la rigenerazione delle cellule TH-positive tramite BDNF e CaMKIIδ3 contro 6-OHDA), wedelolattone ⬖ (regola il proteina neuroprotettiva PD DJ-1/PARK7), dexmedetomidina (neuroprotettiva tramite acetilazione degli istoni mediata da ERK1/2), insieme a 7,8-diidrossiflavone , ⬖ cordicepina ⬖ (contro il rotenone nelle cellule PC12), AMG9810 (un antagonista di TRPV1 che ha ridotto i deficit motori ma ha compromesso la cognizione con l'uso cronico), insulina con inibitore di TLR4 TAK242 (miglioramento delle prestazioni motorie e normalizzazione dell'α-sinucleina nei ratti 6-OHDA), catalpolo ⬖ (riduzione dell'α-sinucleina e miglioramento della funzione mitocondriale contro il rotenone), genisteina , ⬖ decotto di Taohe Siwu , ⬖ composti di Ligusticum chuanxiong ⬖ e acidi grassi di Nigella sativa . ⬖
Poiché il paraquat e altri erbicidi sono tra i più importanti fattori di rischio ambientali per il morbo di Parkinson, è anche degno di nota che il DMSO ha dimostrato, attraverso numerosi studi, di essere in grado di neutralizzare i radicali idrossilici generati dal paraquat, 1 , 2 , 3 , 4 inclusa la prova diretta, ottenuta da studi sui ratti, dell'intercettazione dei radicali idrossilici generati dal paraquat tramite un meccanismo simile alla reazione di Fenton, e, in test con biosensori batterici , di neutralizzare fino al 96% dei radicali superossido generati dal paraquat. È stato inoltre dimostrato che il DMSO ha un effetto neuroprotettivo diretto contro il paraquat in cellule striatali in coltura , sopprime la segnalazione infiammatoria indotta dal paraquat (ad esempio, IL-8 e attività chemiotattica dei neutrofili) e protegge il DNA dalla mutagenesi indotta dal paraquat , fornendo una potenziale spiegazione meccanicistica per il dato epidemiologico secondo cui l'esposizione al DMSO è inversamente associata al rischio di morbo di Parkinson. Inoltre, mirtenolo , ⬖ andrografolide ⬖ (tramite Nrf2/HO-1), VPA (un inibitore di HDAC), chimostatina , propofol e resveratrolo ⬖ ciascuno combinato con DMSO per contrastare la tossicità e lo stress ossidativo indotti dal paraquat in vari modelli tissutali.
Nota: l'aggregazione dell'α-sinucleina in fibrille tossiche è un fattore chiave nella neurodegenerazione del Parkinson. Uno studio ha rilevato che il DMSO allo 0,75-1,0%, soprattutto se combinato con il ferro ferrico, promuove la formazione di oligomeri di α-sinucleina e la citotossicità. Tuttavia, quando il DMSO somministrato per via orale è stato testato su topi vivi (sia topi normali che topi transgenici che sovraesprimevano l'α-sinucleina umana), non è stato rilevato alcun aumento dell'aggregazione dell'α-sinucleina, nessuna perdita neuronale e nessuna patologia simile al Parkinson. Allo stesso modo, non è stato riscontrato che il DMSO iniettato direttamente nella substantia nigra causi perdita di neuroni dopaminergici, accumulo di proteine ubiquitinate o deficit comportamentali 1 , 2 — suggerendo che qualsiasi effetto pro-aggregante il DMSO abbia sull'α-sinucleina nelle colture cellulari isolate (a concentrazioni molto più elevate di quelle che si possono raggiungere in ambito clinico) non si traduca nell'organismo vivente.
Oltre alle evidenze sperimentali, ho ricevuto alcune segnalazioni da lettori e medici che hanno riscontrato benefici con il DMSO. Poiché la mia esperienza si basa principalmente sulla somministrazione endovenosa di DMSO (che ritengo offra i maggiori vantaggi), ho voluto condividere questo campione completo, che include anche approcci non endovenosi, per illustrare la differenza tra di essi.
Una moglie ha descritto cosa è successo quando suo marito, affetto da Parkinson, ha ricevuto una flebo di mannitolo e DMSO durante una terapia con cellule staminali ad Amsterdam: "È sceso da una rampa di scale saltellando senza usare il corrimano, si è tagliato il cibo da solo per una settimana, ha parlato chiaramente, ha aperto le portiere dei taxi". Sapevano che non erano le cellule staminali, che avrebbero impiegato mesi per mostrare risultati.
Il rapporto più dettagliato proviene da un ricercatore scientifico a cui è stato diagnosticato il Parkinson nel 2018, il quale aveva già tenuto sotto controllo i suoi sintomi non motori con il sulforafano α (un attivatore di Nrf2), ma presentava ancora l'intera gamma di sintomi motori. Dopo aver testato sistematicamente il DMSO per via orale per diversi mesi, ha scoperto che a una dose ottimale, la bradicinesia veniva eliminata, il dolore e la distonia ridotti dell'80%, la rigidità ridotta del 50% e i livelli di energia erano nettamente superiori. Ha osservato che il DMSO agiva sui sintomi motori laddove il sulforafano α non era riuscito, suggerendo che il DMSO raggiungesse il cervello in modi che il sulforafano α non poteva, in linea con la nota capacità del DMSO di attraversare la barriera emato-encefalica. In particolare, dosi superiori alla sua soglia peggioravano sistematicamente il tremore, la rigidità e il sonno, ma questi effetti si invertivano completamente entro due giorni dall'interruzione del trattamento.
Una terza persona ha riferito che l'applicazione topica e orale di DMSO inizialmente aveva aiutato il marito affetto da Parkinson a percorrere brevi distanze, ma l'effetto non si era protratto nel tempo.
Inoltre, ho ricevuto anche alcune segnalazioni di persone affette da Parkinson a cui il DMSO assunto per via orale avrebbe aiutato, ma poiché si trattava di informazioni verbali, non posso fornire dettagli specifici al riguardo.
Considerato tutto ciò (e la nostra esperienza con il morbo di Parkinson), credo che il DMSO abbia un grande potenziale per il trattamento di questa patologia: la somministrazione orale è probabilmente più efficace, quella endovenosa lo è ancora di più. Credo inoltre che i risultati migliori si otterranno combinando il DMSO con un agente neurotrofico complementare. Attualmente, ho individuato un candidato molto promettente per questo scopo (insieme ad altre possibilità), ma, come dimostrano gli studi di combinazione sopra citati, è probabile che ce ne siano molti altri ancora da scoprire.
Sclerosi laterale amiotrofica (SLA)
La sclerosi laterale amiotrofica (SLA) è una malattia neurodegenerativa progressiva in cui i motoneuroni che controllano il movimento volontario muoiono gradualmente, causando un progressivo indebolimento muscolare, paralisi e, in genere, la morte entro 2-5 anni dalla diagnosi. Non esiste una cura e i pochi farmaci approvati dalla FDA offrono solo modesti benefici in termini di sopravvivenza. Tuttavia, come dimostra la storia di Todd (in particolare perché era disposto a dimostrare l'efficacia del DMSO interrompendone ripetutamente l'assunzione e documentando poi il rapido peggioramento dei sintomi che ne conseguiva), c'è speranza per la SLA. A sua volta, esistono anche alcune ricerche che lo confermano:
•Nei modelli murini di SLA, la somministrazione orale a lungo termine di DMSO al 5% ha aumentato significativamente il tempo medio di sopravvivenza, ridotto i punteggi neurologici e migliorato le prestazioni motorie (con miglioramenti principalmente funzionali piuttosto che istologici). 1 , 2Nota: il DMSO è stato anche combinato con il riluzolo (uno dei pochi farmaci per la SLA) per trattare una varietà di altre condizioni neurologiche, tra cui il dolore neuropatico, 1 , 2 la degenerazione retinica indotta dalla luce, 1 , 2 la perdita dell'udito (dove è stato anche scoperto che il DMSO da solo protegge l'udito e preserva i neuroni cocleari) e lo stato epilettico , tutte condizioni che i dati dimostrano essere trattate dal DMSO. Inoltre, il DMSO è stato utilizzato come solvente per lo screening di un gran numero di composti per l'uso nella SLA.
• È stato riscontrato che basse concentrazioni di DMSO stabilizzano la conformazione della proteina SOD1 (il ripiegamento errato della SOD1 è una causa centrale della SLA). Inoltre, anche la 5-fluorouridina e l'epigallocatechina gallato ⬖ (che viene spesso combinata con il DMSO) stabilizzano la SOD1.
•Una varietà di agenti in combinazione con DMSO hanno anche mostrato benefici terapeutici nei topi con SLA. Il resveratrolo intraperitoneale cronico ⬖ ha ritardato l'insorgenza della malattia, prolungato la sopravvivenza e preservato quasi il doppio dei motoneuroni. Un inibitore di GSK-3β ha ritardato l'insorgenza della malattia e la morte e ha parzialmente preservato i motoneuroni lombari. Gli inibitori di ASK1 hanno protetto dalla morte dei motoneuroni e ridotto l'attivazione gliale. La rapamicina ha migliorato l'equilibrio neuroprotettivo di fissione/fusione mitocondriale. Il licopene ⬖ ha ridotto in modo dose-dipendente lo stress ossidativo e l'apoptosi dei motoneuroni. In particolare, il carbossimamidotriazolo ha inibito potentemente le citochine infiammatorie in vitro ma non ha migliorato significativamente l'insorgenza o la sopravvivenza rispetto al controllo con veicolo DMSO in vivo, suggerendo potenzialmente che il DMSO stesso stesse già fornendo un beneficio comparabile.
Oltre alla notevole risposta di Todd al DMSO topico e in particolare a quello endovenoso, alcuni altri studi suggeriscono che il DMSO possa essere utile per la SLA e patologie correlate. Un libro racconta di Stanley Jacob che trattò un paziente affetto da SLA con DMSO, ottenendo "miracoli terapeutici immediati, notturni e leggermente ritardati" (dopo i quali il medico proibì ulteriori trattamenti).
Nota: sospetto che questo caso possa essere stato ciò che per primo ha ispirato un mentore a provare il DMSO per via endovenosa per la SLA.
Un altro lettore ha riferito che una sua collega ha somministrato DMSO al padre affetto da SLA ed è rimasta "sorpresa dal visibile miglioramento delle sue condizioni". Infine, un lettore con sindrome da crampi e fascicolazioni (una condizione che si presenta come una SLA in fase iniziale ma non evolve in essa) ha descritto di essere stato spinto al punto di pensare al suicidio dalla combinazione di dolore cronico e grave privazione del sonno, prima di scoprire che il DMSO assunto per via orale migliorava drasticamente l'efficacia degli altri farmaci, permettendogli di dormire tutta la notte, eliminando in gran parte i crampi e il dolore neuropatico e restituendogli la capacità di lavorare e vedere crescere i suoi figli.
Nota: la nostra (limitata) esperienza è che il DMSO per via endovenosa arresta la progressione della SLA, ma non la inverte. Tuttavia, le testimonianze che ho ricevuto suggeriscono che alcuni individui abbiano una risposta considerevolmente più marcata, sia per una predisposizione innata sia per dosi endovenose più elevate. Uno dei miei principali interrogativi irrisolti è se i casi di SLA "atipica" post-vaccino COVID rispondano al DMSO in modo diverso rispetto ai casi di SLA pre-vaccino che avevamo precedentemente riscontrato (da cui proviene tutta la nostra esperienza).
Malattia di Huntington
La malattia di Huntington è una malattia genetica fatale caratterizzata da progressiva perdita del controllo motorio, declino cognitivo e disturbi psichiatrici. Appartiene a una famiglia di nove malattie neurodegenerative (malattie da poliglutamina) causate da proteine mal ripiegate con ripetizioni di glutamina anormalmente lunghe, e una revisione degli chaperoni chimici per queste condizioni ha rilevato che il DMSO ha mostrato una soppressione simile o superiore della tossicità mediata dalla poliglutamina rispetto agli altri chaperoni chimici testati (glicerolo, TMAO). Allo stesso modo, in modelli cellulari della malattia di Machado-Joseph (un altro membro di questa famiglia), il DMSO ha stabilizzato il ripiegamento della proteina mutante atassina-3, riducendo l'aggregazione, la citotossicità e la morte cellulare.
Nell'unico studio che ha testato direttamente il DMSO contro la malattia di Huntington, il DMSO (~1-4%) ha parzialmente prevenuto la morte cellulare, aumentato la vitalità cellulare, diminuito la proteina huntingtina aggregata e aumentato la sua forma solubile (non tossica).
Diversi agenti in combinazione con DMSO hanno anche mostrato benefici terapeutici nei modelli di Huntington. Nei ratti, l'inosina ⬖ ha protetto dai sintomi simili alla malattia di Huntington migliorando la funzione motoria, attivando la via neurotrofica BDNF/TrkB/ERK/CREB, aumentando il BDNF striatale e riducendo lo stress ossidativo, la neuroinfiammazione e il danno neuronale striatale. L'inibizione di FKBP5 ha ridotto i livelli di huntingtina mutata e aumentato la clearance autofagica sia nelle cellule staminali umane di Huntington che nei modelli murini. Nei modelli di Huntington di C. elegans , l'estratto di foglie di olivo ⬖ ha protetto fortemente i neuroni dalla degenerazione indotta da poliglutamina (fino a 4 volte più neuroni intatti) e ha migliorato la risposta meccanosensoriale, mentre il 3-idrossitirosolo ⬖ e il tirosolo ⬖ hanno ridotto il numero di placche di poliglutamina, protetto i neuroni e migliorato la risposta meccanosensoriale. Gli estratti di specie di Hyptis ⬖ hanno anche migliorato significativamente la locomozione e aumentato la resistenza allo stress ossidativo nei modelli di poliglutamina.
Nota: il DMSO è stato utilizzato anche per testare un gran numero di potenziali terapie per la malattia di Huntington e per studiare i suoi meccanismi patogenetici sottostanti .
malattia di Alzheimer
La malattia di Alzheimer (AD), la forma più comune di demenza, è caratterizzata dall'accumulo extracellulare di placche di beta-amiloide (Aβ) (in particolare nell'ippocampo e nella corteccia cerebrale) e di grovigli neurofibrillari intracellulari derivanti dalla proteina tau iperfosforilata. Si ritiene che sia causata dal danno che queste proteine provocano al tessuto cerebrale e, pertanto, praticamente tutta la ricerca sulla malattia si è concentrata sulla rimozione dell'amiloide.
Nota: si può sostenere con forza che le proteine amiloidi proteggano inizialmente le cellule cerebrali dagli agenti stressanti (ad esempio le tossine), come dimostrato dal fatto che tutti i farmaci che eliminano l'amiloide hanno fallito (e spesso presentano effetti collaterali significativi perché inducono il sistema immunitario ad attaccare l'amiloide e quindi a creare infiammazione nel cervello), oltre al fatto che le terapie naturali che agiscono direttamente sui fattori che danneggiano il tessuto cerebrale sono attualmente l'unico trattamento per l'Alzheimer con dati a supporto (ulteriori informazioni sono disponibili qui ).
Il DMSO ha un'utilità unica nella malattia in quanto:
• Stabilizza le proteine ed elimina gli aggregati amiloidi mal ripiegati (consentendo la rimozione di pericolosi accumuli di amiloide in modo non dannoso). Ad esempio, uno studio di modellazione computerizzata ha indicato che il DMSO inibisce l'aggregazione di Aβ modulando la stabilità del ponte salino Lys28-Ala42, mentre le simulazioni di dinamica molecolare hanno mostrato che il DMSO promuove la struttura α-elica e stabilizza Aβ42 (impedendo la formazione del foglietto β che guida l'aggregazione tossica).Nota: uno spray nasale a base di insulina DMSO, sviluppato per il trattamento della malattia di Alzheimer, ha dimostrato nei ratti di rilasciare insulina in tutto il cervello entro un'ora senza segni di tossicità. 1 , 2 , 3
• È un inibitore dell'acetilcolinesterasi, 1 , 2 (la stessa strategia terapeutica utilizzata dai farmaci per l'Alzheimer approvati dalla FDA, donepezil e galantamina).
• È stato dimostrato che aumenta l'attività della fosfatasi alcalina lisosomiale (ALP) del 20%, il che probabilmente migliora la rimozione degli aggregati proteici tossici che contribuiscono alla neurodegenerazione.
Inoltre, le proprietà fondamentali del DMSO (ad esempio, il miglioramento della circolazione, la riduzione dell'infiammazione e il risveglio delle cellule dormienti "danneggiate") contrastano direttamente i processi patologici che causano l'AD. Ad esempio, è stato dimostrato che il DMSO inibisce l'attivazione degli inflammasomi NLRP3 e della caspasi-1, che mediano la neuroinfiammazione cronica che accelera la progressione dell'AD. 1 , 2 , 3
Nota: il DMSO è comunemente utilizzato in laboratorio per solubilizzare e sciogliere i peptidi amiloidi per uso sperimentale, 1 , 2 , 3 , 4 e le condizioni iniziali di solubilizzazione (inclusa l'esposizione al DMSO) influenzano significativamente la riproducibilità della cinetica di aggregazione dell'Aβ . Gli studi che caratterizzano la tossicità di diverse specie di Aβ (oligomeri, protofibrille, fibrille) e frazioni di peso molecolare si sono basati sul DMSO per la preparazione dei peptidi. 1 , 2 Il DMSO è stato anche utilizzato come piattaforma solvente per lo screening di cocktail di farmaci anti-invecchiamento contro la neurotossicità di Aβ e tau in linee cellulari neuronali.
Negli studi sugli animali, il DMSO ha ripetutamente dimostrato benefici cognitivi diretti nei modelli di malattia di Alzheimer:
Nei ratti in cui sono state utilizzate infusioni intracerebroventricolari di streptozotocina (STZ) per modellare l'AD sporadico, la somministrazione giornaliera di DMSO per via endovenosa per 2 settimane ha contrastato il deterioramento della memoria, migliorando le prestazioni nei test comportamentali e di memoria. Ciò è stato corroborato da uno studio in cui la somministrazione cronica intracerebroventricolare di DMSO al 10% (ma non al 2,5% o al 5%) ha attenuato significativamente i deficit di memoria spaziale indotti da STZ nel labirinto acquatico di Morris, con gli autori che hanno attribuito il beneficio alle proprietà antiossidanti, antinfiammatorie e di miglioramento della perfusione cerebrale del DMSO. 1 , 2 In un altro studio su STZ , un gruppo separato ha riscontrato tendenze simili verso una diminuzione della neuroinfiammazione (IL-1β, TNFα), miglioramenti comportamentali e un aumento del BDNF con il trattamento con DMSO.
Nei ratti modello di AD con Aβ25-35 iniettato nell'ippocampo, il DMSO ha migliorato l'apprendimento e la memoria, riducendo la latenza di fuga e la distanza di ricerca nel labirinto acquatico di Morris. In particolare, non è stato osservato alcun effetto sinergico significativo quando il DMSO è stato combinato con l'estratto di Ginkgo biloba, ⬖ suggerendo che il DMSO da solo esercitava già un effetto sostanziale. In uno studio simile , sia il DMSO che l'estratto di Ginkgo biloba ⬖ hanno migliorato l'apprendimento e la memoria nei ratti modello di AD con Aβ25-35, con effetti associati alla modulazione dell'espressione di APP nell'ippocampo.
Inoltre, nei topi geneticamente modificati per sviluppare la malattia di Alzheimer , il DMSO ha aumentato la densità delle spine dendritiche in modo regione-specifico nell'ippocampo, ha migliorato l'accuratezza della memoria spaziale, ha modulato l'assuefazione olfattiva e ha mostrato un effetto ansiolitico. Nonostante questi miglioramenti si siano verificati in animali con livelli elevati di Aβ, il DMSO non ha ridotto le specie oligomeriche di Aβ , e sembra invece agire attraverso la modulazione della segnalazione del recettore NMDA (poiché l'antagonista NMDA MK-801 ha riprodotto l'effetto del DMSO sulla densità delle spine dendritiche), portando gli autori a concludere: " Il DMSO dovrebbe essere considerato un vero e proprio composto bioattivo, che ha il potenziale per essere un utile coadiuvante per contrastare la sinaptotossicità mediata da Aβ e il deterioramento comportamentale " .
In un altro studio sui topi affetti da Alzheimer, il DMSO ha attraversato autonomamente la barriera emato-encefalica, migliorando le funzioni cognitive e riducendo la neuroinfiammazione: effetti osservati nonostante lo studio fosse stato progettato per testare la serpina3n e non il DMSO stesso.
Nei topi giovani (3-4 mesi) geneticamente modificati per sviluppare una forma precoce di Alzheimer, lo 0,01% di DMSO miscelato con l'acqua potabile ha attenuato il declino visivo e l'ispessimento retinico osservati nella fase prodromica dell'Alzheimer (con benefici paragonabili a quelli del R-carvedilolo), indicando che il DMSO ha potenziato il trasporto di acqua dagli occhi, dipendente dall'energia.
Nel C. elegans, il DMSO ha ritardato notevolmente (del 48-98%) la paralisi causata dall'Aβ42 e ha prolungato la durata della vita del 23,0-24,4%. 1 , 2 I ricercatori hanno attribuito il ritardo della paralisi alla modulazione della neurotrasmissione da parte del DMSO , notando che il DMSO ha ridotto la paralisi causata da agenti correlati all'acetilcolina di circa il 70% e che la protezione dipendeva dalla via di longevità daf-16/FOXO.
Nelle colture cellulari, basse concentrazioni di DMSO ( 0,015625–0,0625 %) hanno aumentato la vitalità delle cellule cerebrali e mascherato la tossicità dell'Aβ (concentrazioni facilmente raggiungibili nel tessuto cerebrale assumendo DMSO a casa o con l'uso routinario di DMSO negli esperimenti cellulari).
Nota: poiché il DMSO è usato così frequentemente nella ricerca sull'Alzheimer, è stato ripetutamente proposto che questo effetto protettivo abbia probabilmente contribuito a sovrastimare l'efficacia delle terapie utilizzate con esso e a sottostimare la neurotossicità delle particelle amiloidi. 1 , 2
Inoltre, il DMSO ha modificato lo splicing della proteina precursore dell'amiloide (APP) nell'ippocampo del ratto adulto, favorendo l'isoforma neurotrofica APP-695 (aumentandone la proporzione dall'89% al 94%) e riducendo reciprocamente le isoforme patologiche contenenti KPI (APP-751/770) che sono tipicamente elevate nella malattia di Alzheimer (sottolineando ancora una volta la sua utilità nella malattia). In un modello controllato di trauma cranico nei topi, il DMSO (utilizzato come veicolo per la glibenclamide) ha dimostrato inaspettati effetti benefici indipendenti nelle femmine di topo, riducendo significativamente le proteine patologiche TAU e TDP43 in diverse regioni cerebrali e contribuendo a ripristinare il flusso sanguigno cerebrale (effetti che gli autori dello studio hanno evidenziato come nuovi).
Una revisione giapponese degli anni '80 ha rilevato che il DMSO era stato studiato per sciogliere i depositi di amiloide nei pazienti affetti da Alzheimer, e un rapporto documentava un parziale miglioramento della funzione motoria.
Studi umani
In Moldavia, 18 pazienti con probabile malattia di Alzheimer sono stati trattati con DMSO e sottoposti a test regolari per nove mesi. Si sono notati notevoli miglioramenti già dopo soli tre mesi di trattamento, che sono diventati particolarmente evidenti dopo sei mesi. I miglioramenti hanno riguardato la memoria, la concentrazione e la comunicazione, oltre a una significativa riduzione del disorientamento spazio-temporale.
Analogamente, secondo Jack De La Torre , il principale ricercatore sulle applicazioni neurologiche del DMSO: "Il dimetilsolfossido, un potente antiossidante che è noto per aumentare il flusso sanguigno cerebrale in ambito clinico e sperimentale durante diverse patologie che interessano il cervello, ha dimostrato di migliorare la funzione cognitiva e di stabilizzare gli enzimi proteici nei pazienti affetti da Alzheimer trattati con questo farmaco per 6 mesi".
Nota: non sono riuscito a capire se De La Torre si riferisse allo studio moldavo o a qualcos'altro.
Studi combinati nei modelli di malattia di Alzheimer
Numerose ricerche hanno valutato gli agenti terapeutici disciolti in DMSO in diversi modelli di malattia di Alzheimer.
Elaborazione dell'APP e modulazione della secretasi
Diversi agenti disciolti in DMSO hanno dimostrato la capacità di deviare la processazione dell'APP dalla produzione tossica di Aβ. L'estratto di corteccia di cannella ⬖ ha ridotto la produzione di Aβ40 del 50-60% attraverso i suoi composti attivi medioresinolo e criptamigina A, che hanno diminuito i livelli di β-secretasi. Il levistolide A ⬖ (da Danggui-Shaoyao-San) ha ridotto l'Aβ1-42 extracellulare nelle cellule AD e ha dimostrato di attraversare la barriera emato-encefalica, raggiungendo le concentrazioni cerebrali massime entro 30 minuti. L'apicidina (un inibitore dell'HDAC) ha aumentato l'espressione di ADAM10 (α-secretasi) attraverso la segnalazione USF1 e ERK, deviando la scissione dell'APP dalla via amiloidogenica. L'acido retinoico ha inibito l'attività della γ-secretasi attraverso l'attivazione dell'ERK, mentre i modulatori della γ-secretasi a base di sulfonamidi hanno modificato i rapporti Aβ40/42 senza gli effetti collaterali correlati a Notch dell'inibizione completa della γ-secretasi. Inoltre, diversi inibitori di BACE1 disciolti in DMSO hanno ridotto la produzione di Aβ1-40 e Aβ1-42 nelle cellule neuronali (ma, come altri farmaci amiloidi, hanno fallito nei successivi studi clinici sull'uomo). Il DMSO è stato anche utilizzato per sciogliere l'acido ursolico , che è stato identificato attraverso uno screening ad alto contenuto come un potente inibitore del legame di Aβ al recettore CD36, bloccando la produzione di specie reattive dell'ossigeno da parte della microglia.
Topi transgenici con AD
Le combinazioni di DMSO sono state ampiamente studiate nei topi transgenici AD. La diidromiricetina ⬖ ha migliorato le prestazioni nel labirinto acquatico di Morris, ha ridotto l'accumulo di Aβ e le placche senili e ha ripristinato il flusso autofagico aumentando Beclin1, il rapporto LC3-II/LC3-I e riducendo P62. Numerosi inibitori di HDAC6 hanno alleviato il declino cognitivo, ridotto i livelli di Aβ e la deposizione di placche, diminuito la tau iperfosforilata, aumentato le proteine dell'autofagia e protetto i neuroni corticali dal danno ossidativo. 1 , 2 Un inibitore di p38 MAPK ha migliorato la cognizione riducendo Aβ, la fosforilazione di tau, BACE1 e presenilina, aumentando al contempo le proteine sinaptiche e quelle che degradano l'amiloide. L'astragalina ha migliorato l'apprendimento spaziale e la memoria nei topi riducendo la deposizione di placche di Aβ e potenziando il flusso autofagico tramite la via PI3K/Akt-mTOR. Il ligustilide ha migliorato l'apprendimento e la memoria, promosso il trasporto e la rimozione dell'Aβ e ridotto la neuroinfiammazione. Il blocco cronico del canale TRPA1 ha normalizzato l'attività astrocitaria, prevenuto la disfunzione neuronale, preservato l'integrità sinaptica e impedito il declino della memoria di lavoro spaziale. Il kenpaullone ha migliorato le prestazioni cognitive e ridotto le placche di Aβ, la neurodegenerazione e le citochine proinfiammatorie, mentre l'erlotinib ha migliorato la memoria spaziale a breve termine, aumentato la formazione di spine dendritiche e ridotto la fosforilazione e l'aggregazione della proteina tau.
Tra gli agenti che mirano alla rimozione o alla riduzione dell'Aβ, i nuovi inibitori di c-KIT hanno migliorato la rimozione autofagica di Aβ e tau, l'eriodictiolo ha promosso la rimozione microgliale di Aβ, il mentolo ha inibito la polimerizzazione di Aβ e ridotto le placche senili, e la picropodofillina ha ridotto Aβ e la microgliosi ippocampale, mentre l'acido ellagico ha ridotto sia Aβ che caspasi-3. GTM-1, rapamicina e carbamazepina hanno migliorato la memoria spaziale e ridotto Aβ42 (con GTM-1 che attiva l'autofagia tramite mTOR).
Tra gli agenti che migliorano la funzione sinaptica e la cognizione, un inibitore di JNK ha ridotto l'infiammazione, ripristinato le proteine sinaptiche e migliorato la cognizione; un inibitore di PDE4 ha migliorato la memoria, la plasticità sinaptica e la segnalazione ippocampale; CA140 ha ripristinato la memoria e la funzione sinaptica tramite la segnalazione della dopamina D1; la puerarina ⬖ ha ripristinato l'attività del recettore NMDA; e l'isoliquiritigenina ⬖ ha ripristinato l'equilibrio sinaptico eccitatorio/inibitorio. Un attivatore di SERCA ha migliorato la memoria e la coordinazione motoria, mentre il clenbuterolo ha aumentato PSA-NCAM e migliorato la cognizione.
Altri agenti che agiscono attraverso la neuroprotezione, la neurogenesi o la modulazione immunitaria includono un agonista LXR (che ha promosso la neurogenesi e aumentato l'espressione di apoE), un agonista CB2R (che ha spostato la microglia da M1 a M2 antinfiammatoria), l'idebenone (che ha migliorato la memoria spaziale e la funzione mitocondriale), un agonista del recettore degli estrogeni beta e la berberina ⬖ (che ha ridotto l'apoptosi e aumentato l'espressione di Bcl-2 nei neuroni dell'ippocampo in modo dose-dipendente).
Modelli AD sporadici
Anche i modelli di AD sporadica (utilizzando STZ intracerebroventricolare) hanno risposto alle terapie di combinazione. Un derivato della triazina ha migliorato l'apprendimento spaziale e aumentato lo spessore dello strato piramidale dell'ippocampo, la canagliflozina ha migliorato la morfologia dendritica, l' estratto di Croton hirtus ⬖ MECH ha invertito i deficit di apprendimento e memoria riducendo al contempo Aβ e AChE, e la rapamicina ha ridotto la tau iperfosforilata e la segnalazione mTOR. L' inibitore di MIF ISO-1 ha migliorato la memoria contestuale dipendente dall'ippocampo e ridotto la produzione di citochine, con livelli di MIF riscontrati elevati nel liquido cerebrospinale di pazienti con AD in fase iniziale. L' inibitore di GSK-3β SB216763 ha attenuato l'UPR indotta da tunicamicina, i deficit sinaptici e i deficit di memoria.
Modelli di iniezione acuta di Aβ
I modelli di iniezione acuta di Aβ sono stati utilizzati per testare una vasta gamma di agenti. L'estratto di Piper kadsura ohwi ⬖ ha migliorato significativamente i deficit etologici sia degli oligomeri di Aβ che dell'Aβ fibrillare, riducendo al contempo la neuroinfiammazione tramite TLR4/NF-κB/TNF-α. 1 , 2 La rapamicina ha migliorato la funzione cognitiva, ridotto la deposizione di Aβ nell'ippocampo e aumentato l'espressione di Homer3. Il testosterone ha invertito i deficit di apprendimento spaziale e la perdita neuronale tramite la segnalazione BDNF/CaMKII/CREB (un effetto completamente bloccato dall'antagonista del recettore degli androgeni flutamide). La curcumina ⬖ disciolta in DMSO ha parzialmente migliorato l'apprendimento spaziale nei ratti modello di AD e ha anche invertito il danno indotto da Aβ alle cellule staminali neurali, migliorando la vitalità e i marcatori di differenziazione (Nestin, Tuj-1, GFAP). 1 , 2 , 3 Il pioglitazone ha invertito in modo dose-dipendente l'attivazione di MKK4, JNK1 e c-Jun indotta da Aβ1-42 nell'ippocampo del ratto, con la maggior parte dell'immunoreattività di p-JNK che si localizza insieme alla microglia.
Altri agenti che hanno migliorato la cognizione o ridotto la patologia dell'AD nei modelli con iniezione di Aβ includono l'estratto di Angelica keiskei ⬖ (che ha migliorato la memoria in modo dose-dipendente), la genisteina a basso dosaggio ⬖ (che ha aumentato l'espressione di STAT3 e soppresso la caspasi-3), l'acido betulinico ⬖ (che ha migliorato la memoria, l'ansia e la LTP), il DL0410 (un doppio inibitore di AChE/BChE che ha migliorato l'apprendimento tramite CREB/BDNF), l'estratto di foglie di B. pendula ⬖ (che ha ridotto lo stress ossidativo e la segnalazione NF-κB), il decotto di Huanglian Jiedu ⬖ (che ha ridotto l'attivazione microgliale), un inibitore di DAPK1 (che ha ridotto l'attivazione dell'inflammasoma NLRP3 e migliorato i deficit di memoria) e l'atorvastatina (che ha prevenuto la sinaptotossicità e la neuroinfiammazione tramite l'inibizione di p38 MAPK). La biochanina A ⬖ ha attenuato la morte neuronale indotta da Aβ e migliorato l'apprendimento spaziale tramite l'inibizione della p38 MAPK dipendente dal recettore degli estrogeni, mentre la frazione esanica di Perilla frutescens ⬖ ha inibito l'aggregazione di Aβ e protetto le cellule dalla tossicità di Aβ, così come un peptide rompi-foglietto beta appositamente progettato .
Altri agenti che mostrano effetti neuroprotettivi nei modelli cellulari Aβ includono gli alcaloidi di Dendrobium nobile ⬖ (che hanno aumentato la sopravvivenza cellulare), la neuroprotectina D1 (che ha ridotto Aβ42, la fosforilazione di tau e l'apoptosi mentre potenziava l'autofagia), la curcumina ⬖ (che ha ridotto i ROS mitocondriali, potenziato l'autofagia tramite le proteine Rab e aumentato il trasporto assonale), 1 , 2 , 3 l'icariina ⬖ (che ha inibito l'autofagia e ridotto la produzione di Aβ tramite p70 S6K), un inibitore della DPP-4 (che ha attivato PI3K/Akt/GSK-3β e ridotto la fosforilazione di tau), il ferulato di sodio ⬖ (che ha protetto i neuroni ippocampali tramite la modulazione della via Notch), il butilftalide (che ha protetto le cellule endoteliali dall'apoptosi indotta da Aβ tramite TLR4/COX-2), 1 , 2 ZL006 (che ha attivato Akt/Nrf2/HO-1), MS-275 e JQ1 (che hanno migliorato la memoria tramite CREB e ridotto il TNF-α), pioglitazone (che ha ridotto Aβ e tau tramite l'attivazione di PPARγ), tetraidrossistilbene glucoside ⬖ (che ha ridotto l'infiammazione microgliale e l'espressione di APOE/TREM2), berberina ⬖ (che ha promosso la polarizzazione M2 microgliale tramite la segnalazione PI3K-AKT, proteggendo i neuroni dal danno mediato da Aβ) e inibizione del recettore 5-HT1B (che ha ripristinato la fosforilazione di eNOS e Akt alterata da Aβ1-42 nelle cellule endoteliali umane, suggerendo che questo recettore media la disfunzione vascolare indotta da Aβ rilevante per l'AD).
Modelli dell'acido okadaico (OA)
Anche i modelli di acido okadaico (che inducono l'iperfosforilazione della proteina tau inibendo la proteina fosfatasi 2A) hanno risposto alle terapie somministrate tramite DMSO. Il decotto di Trillium tschonoskii ⬖ ha migliorato l'apprendimento spaziale, aumentato l'attività della PP2A e ridotto la fosforilazione della proteina tau preservando i neuroni dell'ippocampo. Il decotto di Banqiao Codonopsis pilosula ⬖ ha migliorato la cognizione in modo dose-dipendente, ridotto l'iperfosforilazione della proteina tau e aumentato le proteine sinaptiche e il numero di spine dendritiche. 1 , 2 Nel pesce zebra, il Mansonone G ⬖ ha invertito le alterazioni cognitive indotte dall'OA, migliorando la memoria spaziale e di riconoscimento e ripristinando la funzione colinergica. Altri agenti includono il ginsenoside Rb1 ⬖ (che ha attenuato l'iperfosforilazione della proteina tau), il ginkgolide ⬖ combinato con l'insulina (che ha migliorato sinergicamente l'apprendimento e ridotto i grovigli neurofibrillari), il polipeptide di corna di cervo pelose ⬖ (che ha attivato PI3K/AKT e ridotto l'apoptosi) e la sarsasapogenina ⬖ (che ha attenuato l'iperfosforilazione della proteina tau tramite Akt/GSK-3β).
Patologia della proteina Tau
Diverse scoperte riguardano direttamente la proteina tau, un fattore chiave nella neurodegenerazione causata dalla malattia di Alzheimer:
Nei topi femmina dopo un trauma cranico, il DMSO ha ridotto in modo indipendente le proteine patologiche TAU e TDP43 in diverse regioni cerebrali, un effetto paragonabile alla glibenclamide. L'EGTA (un chelante del calcio) ha diminuito la fosforilazione della proteina tau a Ser396 nei topi con malattia di Alzheimer riducendo l'espressione di calpaina 2 e CDK5. Il resveratrolo ha ridotto l'iperfosforilazione della proteina tau indotta dal cadmio tramite l'attivazione di AMPK/PI3K/Akt, mentre il resveratrolo ha anche ridotto l'acetilazione e la fosforilazione della proteina tau nei ratti anziani con disfunzione cognitiva postoperatoria attivando SIRT1 e spostando la microglia dal fenotipo M1 al fenotipo M2a. 1 , 2 L' acido docosaesaenoico somministrato dopo un trauma cranico ha ridotto la proteina tau fosforilata e l'accumulo di APP. L'inibizione di UCH-L1 ha bloccato la formazione di aggresomi di tau riducendo le catene di ubiquitina legate a K63 e compromettendo il legame tra HDAC6 e tau.
In C. elegans (ceppi AD) l'estratto di canapa ⬖ (contenente sia cannabinoidi che terpeni, dispersi in DMSO) ha aumentato significativamente la durata della vita nei nematodi modello tau, con il CBD ⬖ che ostacola direttamente la formazione di aggregati proteici.
Stress ossidativo
L'estere etilico dell'acido ferulico , somministrato per via intraperitoneale in DMSO, ha protetto i sinaptosomi del cervello del gerbillo dal danno ossidativo indotto da Aβ, riducendo le specie reattive dell'ossigeno, l'ossidazione proteica e la perossidazione lipidica, potenziando al contempo le difese antiossidanti (HO-1, HSP72) e riducendo l'iNOS. L' astaxantina ha migliorato in modo dose-dipendente le prestazioni cognitive, ridotto l'accumulo di Aβ42 e malondialdeide, inibito le attività di AChE e MAO e aumentato l'espressione di Nrf2 e miR-124. Nei topi , il DMSO ha ridotto le ROS cerebrali del 9,8-79% (effetto maggiore nei topi giovani) e il danno proteico ossidativo irreversibile del 30,7-69% (effetto maggiore nei topi anziani); questi benefici sono stati ulteriormente potenziati dalla curcumina. ⬖ Nei ratti, l'inibizione di SIRT2 ha ridotto lo stress ossidativo, aumentato l'anti-apoptotico bcl-2 e innalzato il regolatore dell'autofagia beclin-1 nella corteccia e nell'ippocampo, mentre la melatonina ⬖ e la curcumina ⬖ hanno entrambe ridotto la perossidazione lipidica e l'espressione di SIRT2 e aumentato Nrf2 e le difese antiossidanti nella corteccia cerebrale (sebbene senza effetto sinergico quando combinate).
MSM ⬖ (metabolita ossidato del DMSO) ha migliorato la neurodegenerazione indotta dalla co-esposizione a BPA e radiazioni, riducendo i marcatori di AD (Aβ42 del 71,6%, AChE di circa il 50%, fosforilazione della proteina tau del 57%), aumentando il BDNF (132-160%), sopprimendo la via TREM-2/DAP12 e riducendo le placche di Aβ di circa il 75%.
Nota: l'MSM ⬖ attraversa rapidamente la barriera emato-encefalica (rilevabile entro ~10 minuti dall'assunzione orale), raggiungendo concentrazioni cerebrali di ~2,36 mM dopo l'integrazione orale con un'emivita di circa 7,5 giorni. 1 , 2
Inibizione dell'acetilcolinesterasi e screening farmacologico
Oltre al DMSO stesso, che è un inibitore dell'AChE, diversi inibitori dell'AChE sono stati testati in DMSO per la loro rilevanza nella malattia di Alzheimer. Nuovi derivati dell'acido tacrina-idrossamico hanno mostrato una potente doppia inibizione dell'AChE/HDAC con inibizione dell'Aβ, mentre gli inibitori a base di tiazolo hanno superato la rivastigmina e l'uperzina-A. Tra i 21 flavonoidi analizzati, la galangina ha mostrato la più forte inibizione dell'AChE cerebrale (IC50 ~120 μM). Un altro screening ha identificato una sonda multifunzionale che (con DMSO) si lega agli aggregati di Aβ, inibisce la colinesterasi e migliora la memoria cognitiva e spaziale.
Composti naturali e organismi modello
Una vasta gamma di composti naturali disciolti in DMSO ha mostrato effetti neuroprotettivi nei modelli di AD. In C. elegans, l'estratto di foglie d'olivo ⬖ ha protetto fortemente i neuroni dalla degenerazione indotta da Aβ, mentre il 3-idrossitirosolo, ⬖ il tirosolo, ⬖ lo zafferano, ⬖ il Polygonum multiflorum, ⬖ e lo Ziziphus jujuba ⬖ hanno fornito ciascuno una protezione significativa. 1 Il cannabidiolo ⬖ ha prolungato la durata della vita e rallentato il deterioramento neuronale correlato all'età in C. elegans e ha migliorato la crescita dei neuriti e la densità delle spine dendritiche nei neuroni dei mammiferi attraverso la stessa via SIRT1. La quercetina ⬖ e la rifampicina hanno ridotto individualmente le placche di Aβ, con la combinazione che ha prodotto la maggiore eliminazione. La quercetina ⬖ e il kaempferolo ⬖ (polifenoli isolati da colture cellulari di Ginkgo biloba) hanno ridotto in modo dose-dipendente la carbonilazione proteica in C. elegans, un marcatore chiave del danno proteico correlato all'invecchiamento e legato alle malattie neurodegenerative. Gli ibridi di ossoisoaporfina-acido lipoico hanno migliorato l'apprendimento, la memoria, la durata della vita e l'inibizione dell'AChE in Drosophila transgenica Aβ42. Nel pesce zebra, gli antagonisti dei recettori purinergici (caffeina, ZM241385, DPCPX) hanno impedito il deterioramento della memoria indotto dalla scopolamina.
In modelli cellulari e animali, il carvacrolo ⬖ ha protetto i neuroni dalla neurotossicità indotta da Aβ e ha migliorato la memoria nei ratti AD, 1 , 2 mentre i withanolidi derivati dall'ashwagandha ⬖ hanno ripristinato la lunghezza degli assoni/dendriti e i marcatori sinaptici nei neuroni danneggiati da Aβ e hanno invertito i deficit di memoria quando somministrati per via orale. Gli estratti di Cynarae folium ⬖ hanno mostrato effetti neuroprotettivi contro l'Aβ sia nelle cellule che nei ratti, mentre nelle mosche Aβ resistenti ai farmaci, l'anle138b ha prolungato significativamente la sopravvivenza. L'estratto di Ptychopetalum olacoides ha invertito l'amnesia indotta da MK-801, suggerendo il coinvolgimento del sistema glutamatergico nelle sue proprietà di miglioramento cognitivo.
Altri composti naturali che mostrano effetti anti-Aβ includono la curcumina ⬖ 1 , 2 (che ha soppresso la segnalazione microgliale HMGB1/RAGE/NF-κB), la bisdemetossicurcumina , ⬖ polifenoli di Ginkgo biloba ⬖ (che hanno protetto le cellule dPC12 dal danno da Aβ), Perilla frutescens ⬖ (che ha disaggregato gli aggregati di Aβ preformati), l'icariina ⬖ (che ha ridotto iNOS e TNF-α e migliorato la cognizione nei topi AD indotti da LPS), vari estratti di germogli commestibili ⬖ 1 , 2 , 3 (con i germogli di grano saraceno ⬖ che mostrano la più forte soppressione di ROS e riduzione di Aβ), la curcumina ⬖ (che, legandosi all'amiloide, ha consentito il rilevamento in vivo dell'amiloide retinica in topi AD transgenici vivi tramite oftalmoscopia confocale, dimostrando il potenziale per l'AD non invasivo diagnosi), e i polifenoli acido nordiidroguaiaretico, ⬖ baicaleina, ⬖ ed estratto di Padina ⬖ (che hanno protetto le cellule dal danno indotto da Aβ42). La curcumina ⬖ disciolta in DMSO ha inoltre raggiunto un'elevata solubilità nel siero (almeno 3 mM), inibendo efficacemente la formazione di placche di Aβ.
Modelli di malattia di Alzheimer legata all'invecchiamento
L'iniezione di D-galattosio crea un invecchiamento accelerato nei roditori che simula il declino cognitivo legato all'età. Il Guilingji ⬖ (una formula tradizionale) ha migliorato significativamente le prestazioni nel labirinto acquatico di Morris nei ratti invecchiati con D-galattosio, ripristinando l'attività antiossidante e normalizzando i neurotrasmettitori. L'estratto di Ganoderma tsugae ⬖ ha migliorato la locomozione, l'apprendimento e la memoria aumentando gli enzimi antiossidanti cerebrali e il BDNF, riducendo al contempo l'attivazione dell'inflammasoma. Il Kurarinone ⬖, combinato con l'esercizio riabilitativo, ha migliorato sinergicamente l'apprendimento spaziale e la memoria, ha aumentato i marcatori di plasticità sinaptica (PSD-95, sinaptofisina) e ha ridotto la deposizione di Aβ1-42 tramite la via BACE1/Aβ. Il resveratrolo ⬖ ha aumentato significativamente la SOD e diminuito il danno ossidativo nei neuroni dell'ippocampo di topi con invecchiamento indotto da D-galattosio. La curcumina ⬖ ha ridotto l'espressione di APP e tau e ha soppresso l'attività HAT nei ratti AD. L'artemisinina ⬖ ha inoltre dimostrato effetti neuroprotettivi in un modello animale di prevenzione dell'Alzheimer.
Il cloruro di alluminio, che induce l'accumulo di placche di Aβ e la fosforilazione della proteina tau, è stato contrastato da un derivato del bitiofene che ha ripristinato le difese antiossidanti, prevenuto la perdita neuronale e sinaptica e attenuato la patologia correlata all'Alzheimer. 1 , 2
Demenza vascolare
La demenza vascolare (VaD) è causata da un'ipoperfusione cerebrale cronica che provoca danni neuronali progressivi e declino cognitivo, rendendo il DMSO particolarmente adatto al trattamento di questa patologia.
Due inibitori della p38 MAPK disciolti in DMSO hanno ripetutamente migliorato l'apprendimento spaziale e la memoria nei ratti con VaD indotta da occlusione bilaterale dell'arteria carotide, riducendo l'apoptosi ippocampale, prolungando la sopravvivenza e diminuendo la fosforilazione della p38 MAPK. 1 , 2 , 3 La curcumina ⬖ disciolta in DMSO ha migliorato in modo dose-dipendente l'apprendimento e la memoria nei ratti con VaD indotta da occlusione bilaterale dell'arteria carotide, riducendo la patologia ippocampale e promuovendo l'efflusso di colesterolo cerebrale attraverso la via LXR/RXR-ABCA1-apoA1. 1 , 2 , 3 La paeoniflorina ⬖ ha migliorato l'apprendimento e la memoria nei ratti VaD riducendo le citochine proinfiammatorie e inducendo la polarizzazione microgliale da M1 a M2 tramite il recettore cannabinoide di tipo 2. L'inibizione della catepsina B ha ridotto le anomalie mitocondriali, l'apoptosi neuronale, la neuroinfiammazione e la disfunzione cognitiva dopo l'occlusione transitoria dell'arteria cerebrale media.
Ulteriori agenti che migliorano la cognizione nei modelli VaD includono andrografolide ⬖ (che ha ridotto l'apoptosi ippocampale e aumentato Bcl-2), PGE1 (che ha migliorato l'apprendimento e la memoria tramite la via BDNF/TrkB), esketamina (che ha aumentato BDNF, ERK e Nrf2), tripclorolide ⬖ (che ha ridotto Aβ, NF-κB e COX-2), IGF-1 (che ha migliorato la cognizione tramite Akt/mTOR), eritropoietina ricombinante intranasale (che ha migliorato la latenza di fuga e preservato i neuroni ippocampali), la formula Shenmayizhi ⬖ (che ha aumentato le proteine sinaptiche e VEGF), resveratrolo con attivazione SIRT1 (che ha migliorato la cognizione e aumentato la capacità antiossidante nell'ischemia cerebrale cronica), composto inibitore HDAC 13 (che ha attivato le isoforme BDNF e modulato la segnalazione del recettore AMPA), rapamicina (che ha invertito Soppressione dell'autofagia mediata da mTOR, riduzione dell'accumulo di Aβ e iperfosforilazione di tau nei ratti diabetici dopo chirurgia ortopedica), ed emodina ⬖ (che ha ridotto i ROS e inibito la proliferazione neointimale nella stenosi dell'arteria carotide). La quercetina ⬖ ha anche alleviato la demielinizzazione ippocampale in un modello di stenosi bilaterale dell'arteria carotide.
Nota: la perdita dei molari (estrazione dentale) nei ratti con demenza vascolare ha peggiorato il deficit cognitivo e aumentato l'apoptosi ippocampale e l'espressione di iNOS/p38 MAPK/NF-κB; un inibitore di p38 MAPK in DMSO ha ridotto questi effetti, dimostrando che la salute dentale ha un impatto sul declino cognitivo cerebrovascolare.
Il DMSO è stato anche utilizzato per differenziare le cellule staminali mesenchimali del midollo osseo (BMSC) in cellule simili a neuroni che esprimono marcatori neuronali (utilizzando un mezzo DMSO/BHA al 2%), che sono state poi trapiantate nel cervello di ratti affetti da VaD, e le BMSC hanno promosso il recupero di un modello cellulare di AD mediante la sovraregolazione del PDGF-BB attraverso la via PI3K/AKT.
La moglie di mio zio soffre di demenza e non riesce a parlare da oltre un anno. Mia madre è andata a trovarli di recente e ha parlato loro del DMSO. Mio zio ha iniziato a somministrare il DMSO alla moglie per via orale. Dopo due settimane, lei ha ricominciato a parlare.PRIMA PARTE : I. Come il DMSO guarisce il cervello e trasforma la neurologia
Ho letto l'articolo e ho iniziato a somministrarlo a mia madre di 93 anni, mescolandolo al suo succo di frutta ogni mattina, a partire dalla fine di novembre. Soffre di una qualche forma di demenza da oltre 15 anni. Nell'ultimo anno circa, aveva avuto episodi molto gravi di "sundowning" (declino del sonno) e non riusciva a seguire le istruzioni. Da quando assume il DMSO, non soffre più di questi episodi. È più lucida e riesce a comunicare e a ridere con noi. Ha ritrovato la sua personalità. Capisce quando le chiedo di andare in bagno. Le sue capacità cognitive sono migliorate e ha ricominciato a colorare i suoi libri da colorare.
Apprezzo moltissimo i tuoi post sul DMSO . Hai contribuito a far tornare l'interazione spontanea nella vita di mio padre affetto da Alzheimer, così come a quella di molte altre persone a cui ho fornito informazioni sui suoi usi. Che Dio ti benedica.
Nel frattempo, le tue informazioni sul DMSO sembrano aver cambiato radicalmente la situazione per lui [un paziente colpito da ictus]. Siamo a circa otto settimane dall'inizio del trattamento e ho osservato che: la voce è più forte, il linguaggio è nettamente migliorato, l'appetito è aumentato, la disfagia è cambiata drasticamente: ora è in grado di mangiare pasti di dimensioni normali. Ora si nutre quasi esclusivamente da solo, usando la mano colpita. Il suo senso del gusto ha iniziato a tornare.
Abbiamo provato diverse delle terapie che ci avete consigliato. Ho iniziato ad aggiungere 2/3 di cucchiaino di DMSO con un cucchiaino di galattosio ⬖ al suo caffè ogni mattina. Ho iniziato a dargli 2 cucchiaini dopo colazione nel succo di frutta e altri 2 cucchiaini nel pomeriggio, con buoni risultati. È guarito? NO, ma sta molto meglio.
Infine, un lettore ha condiviso la storia del suo compagno (75 anni) a cui era stato diagnosticato un glioblastoma inoperabile di 8 cm, che aveva causato una lenta emorragia cerebrale, la perdita della capacità di parlare e una paralisi del lato destro, con una prognosi di 3 settimane di vita. Dopo abbondanti applicazioni topiche di DMSO al 99%, la funzione motoria ha iniziato a tornare entro 24 ore. Alla terza settimana, mangiava già a tavola. Alla quarta settimana, riusciva a camminare con un deambulatore. Una nuova TAC al 55° giorno non ha mostrato emorragia cerebrale e ha evidenziato una riduzione delle dimensioni del tumore.
https://sadefenza.blogspot.com/2026/04/come-il-dmso-guarisce-il-cervello-e.html
TERZA PARTE : III. DMSO e Sclerosi multipla






Nessun commento:
Posta un commento